Bevandenės savybės, jų formavimas, nomenklatūra, taikymas
The anhidridai jie yra cheminiai junginiai, kilę iš dviejų molekulių sujungimo per vandenį. Taigi jis gali būti laikomas pradinių medžiagų dehidratacija; nors tai nėra tiesa.
Organinėje ir neorganinėje chemijoje jie paminėti, ir abiejose šakose jų suvokimas skiriasi žymiai. Pavyzdžiui, neorganinėje chemijoje baziniai ir rūgštiniai oksidai laikomi atitinkamai jų hidroksidų ir rūgščių anhidridais, nes pirmasis reaguoja su vandeniu ir sudaro pastarąjį..

Čia gali atsirasti painiavos tarp terminų „bevandenis“ ir „anhidridas“. Paprastai bevandenis reiškia junginį, kuris buvo dehidratuotas be cheminio pobūdžio pokyčių (be reakcijos); kadangi su anhidridu yra cheminių pokyčių, atspindinčių molekulinę struktūrą.
Jei hidroksidai ir rūgštys yra lyginami su jų atitinkamais oksidais (arba anhidridais), pastebima, kad reakcija įvyko. Priešingai, kai kurie oksidai ar druskos gali būti hidratuoti, prarasti vandenį ir lieka tie patys junginiai; bet be vandens, ty bevandenio.
Kita vertus, organinės chemijos atveju tai, kas yra anhidridas, yra pradinis apibrėžimas. Pavyzdžiui, vienas iš labiausiai žinomų anhidridų yra karboksirūgščių dariniai (viršutinis vaizdas). Tai susideda iš dviejų acilo grupių (-RCO) sujungimo deguonies atomu.
Bendrojoje struktūroje nurodoma R1 acilo grupei ir R2 antrosios acilo grupės. Kadangi R1 ir R2 jie yra skirtingi, jie kilę iš skirtingų karboksirūgščių ir yra asimetrinis rūgšties anhidridas. Kai abu R pakaitalai (nepriklausomai nuo to, ar jie yra aromatiniai) yra tokie patys, šiuo atveju kalbame apie simetrišką rūgšties anhidridą..
Tuo metu, kai dvi karboksirūgštys susiejamos su anhidridu, vanduo gali susidaryti arba nebūti, taip pat kiti junginiai. Viskas priklausys nuo minėtų rūgščių struktūros.
Indeksas
- 1 Anhidridų savybės
- 1.1 Cheminės reakcijos
- 2 Kaip susidaro anhidridai?
- 2.1 Cikliniai anhidridai
- 3 Nomenklatūra
- 4 Programos
- 4.1 Organiniai anhidridai
- 5 Pavyzdžiai
- 5.1 Gintaro rūgšties anhidridas
- 5.2 Glutaro rūgšties anhidridas
- 6 Nuorodos
Anhidridų savybės
Anhidridų savybės priklausys nuo to, ką jūs nurodote. Beveik visi turi bendrą, kad jie reaguoja su vandeniu. Tačiau vadinamosiose bazinių anhidridų, esančių neorganinėse medžiagose, iš tikrųjų keletas iš jų net netirpsta vandenyje (MgO), todėl šis teiginys bus sutelktas į karboksirūgščių anhidridus..
Lydymosi ir virimo temperatūros priklauso nuo molekulinės struktūros ir tarpmolekulinės sąveikos (RCO).2Arba tai yra bendra šių organinių junginių cheminė formulė.
Jei molekulinė masė (RCO)2Arba jis yra mažas, tikriausiai yra bespalvis skystis kambario temperatūroje ir slėgyje. Pavyzdžiui, acto anhidridas (arba etano rūgšties anhidridas), (CH3CO)2Arba tai yra skystis ir pramoninės svarbos skystis.
Reakciją tarp acto rūgšties anhidrido ir vandens sudaro tokia cheminė lygtis:
(CH3CO)2O + H2O => 2CH3COOH
Atkreipkite dėmesį, kad pridėjus vandens molekulę, išsiskiria dvi acto rūgšties molekulės. Tačiau atvirkštinė reakcija negali vykti acto rūgščiai:
2CH3COOH => (CH3CO)2O + H2O (tai neįvyksta)
Būtina kreiptis į kitą sintetinį maršrutą. Kita vertus, dikarboksirūgštys gali tai padaryti kaitinant; bet tai bus paaiškinta kitame skyriuje.
Cheminės reakcijos
Hidrolizė
Viena iš paprasčiausių anhidridų reakcijų yra jų hidrolizė, kuri ką tik buvo parodyta acto rūgšties anhidridui. Be šio pavyzdžio, turime sieros rūgšties anhidridą:
H2S2O7 + H2O <=> 2H2SO4
Čia yra neorganinio rūgšties anhidridas. Atkreipkite dėmesį, kad H2S2O7 (dar vadinama disulfato rūgštimi), pati reakcija yra grįžtama, todėl šildymas H2SO4 Koncentratas sukuria jo anhidridą. Kita vertus, tai yra atskiestas H tirpalas2SO4, SO yra išleistas3, sieros anhidridas.
Esterifikacija
Rūgštiniai anhidridai reaguoja su alkoholiais, terpėje yra piridinas, kad gautų esterį ir karboksirūgštį. Pavyzdžiui, atsižvelgiama į acto rūgšties anhidrido ir etanolio reakciją:
(CH3CO)2O + CH3CH2OH => CH3CO2CH2CH3 + CH3COOH
Taip susidaro etilo esterio etanoatas, CH3CO2CH2CH3, ir etano rūgštis (acto rūgštis).
Praktiškai atsitinka hidroksilo grupės vandenilio pakaitalas acilo grupėje:
R1-OH => R1-OCOR2
(CH3CO)2Arba jūsų acilo grupė yra -COCH3. Todėl sakoma, kad OH grupė patiria acilinimą. Tačiau acilinimas ir esterinimas nėra keičiamos sąvokos; Acilinimas gali vykti tiesiogiai aromatiniame žiede, žinomas kaip Friedel-Crafts acilinimas.
Taigi alkoholiai, kuriuose yra rūgščių anhidridų, esterinami acilinimo būdu.
Kita vertus, tik vienas iš dviejų acilo grupių reaguoja su alkoholiu, kiti lieka vandeniliu, sudarant karboksirūgštį; kad (CH3CO)2Arba tai yra etano rūgštis.
Amidacija
Rūgštiniai anhidridai reaguoja su amoniaku arba aminais (pirminiais ir antriniais), kad gautų amidus. Reakcija yra labai panaši į ką tik aprašytą esterinimą, bet ROH yra pakeistas aminu; pavyzdžiui, antrinis aminas, R2NH.
Vėlgi, reakcija tarp (CH3CO)2O ir dietilaminas, Et2NH:
(CH3CO)2O + 2Et2NH => CH3CONEt2 + CH3COO-+NH2Et2
Suformuojami dietilacetamidas, CH3CONEt2, ir karboksilo amonio druska, CH3COO-+NH2Et2.
Nors lygtis gali atrodyti šiek tiek sunku suprasti, pakanka stebėti, kaip grupė -COCH3 pakeisti Et2NH sudaro amidą:
Et2NH => Et2NCOCH3
Daugiau nei amidacija reakcija vis dar yra acilinimas. Viskas apibendrinta šiame žodyje; šiuo metu aminas kenčia nuo acilinimo, o ne alkoholio.
Kaip susidaro anhidridai?
Neorganiniai anhidridai susidaro reaguojant su deguonimi. Taigi, jei elementas yra metalinis, susidaro bazinis metalo oksidas arba anhidridas; ir jei jis yra nemetalinis, susidaro nemetalo oksidas arba rūgšties anhidridas.
Organinių anhidridų reakcija skiriasi. Du karboksirūgštys negali tiesiogiai prisijungti prie vandens ir susidaro rūgšties anhidridas; reikalingas dar neišvardyto junginio dalyvavimas: acilo chloridas, RCOCl.
Karboksirūgštis reaguoja su acilo chloridu, gamindama atitinkamą anhidridą ir vandenilio chloridą:
R1COCl + R2COOH => (R1CO) O (COR2) + HCl
CH3COCl + CH3COOH => (CH3CO)2O + HCl
A CH3 kilęs iš acetilo grupės, CH3CO, o kitas jau yra acto rūgštyje. Konkretaus acilo chlorido, taip pat karboksirūgšties pasirinkimas gali sukelti simetriško arba asimetrinio rūgšties anhidrido sintezę..
Cikliniai anhidridai
Skirtingai nuo kitų karboksirūgščių, kurioms reikalingas acilo chloridas, dikarboksirūgštys gali būti kondensuotos atitinkamame jų anhidride. Tam reikia juos šildyti, kad būtų skatinamas H2Pavyzdžiui, parodyta ftalio rūgšties susidarymas ftalio rūgštyje.

Atkreipkite dėmesį, kaip baigtas penkiakampis žiedas, ir deguonis, kuris jungia abi grupes C = O, yra jo dalis; Tai yra ciklinis anhidridas. Taip pat matyti, kad ftalio anhidridas yra simetriškas anhidridas, nes abu yra R1 kaip R2 Jie yra identiški: aromatinis žiedas.
Ne visos dikarboksirūgštys gali sudaryti jų anhidridą, nes, kai jų COOH grupės yra plačiai atskirtos, jos yra priverstos užpildyti didesnius ir didesnius žiedus. Didžiausias žiedas, kurį galima sudaryti, yra šešiakampė, didesnė nei reakcija.
Nomenklatūra
Kaip įvardijami anhidridai? Nepaisant neorganinių medžiagų, susijusių su oksidais, iki šiol paaiškintų organinių anhidridų pavadinimai priklauso nuo R identiteto.1 ir R2; tai yra, jo acilo grupės.
Jei du R yra vienodi, pakanka pakeisti žodį „rūgštis“ „anhidridui“ atitinkamame karboksirūgšties pavadinime. Ir jei, priešingai, abi R yra skirtingos, jos pavadintos abėcėlės tvarka. Todėl, norint žinoti, ką tai vadinti, pirmiausia reikia pamatyti, ar tai yra simetriškas ar asimetrinis rūgšties anhidridas.
(CH3CO)2Arba tai yra simetriška, nes R1= R2 = CH3. Acto arba etano rūgšties darinys, todėl jo pavadinimas yra, remiantis ankstesniu paaiškinimu: acto rūgšties anhidridas arba etano rūgštis. Tas pats pasakytina ir apie ką tik paminėtą ftalio anhidridą.
Tarkime, kad turite tokį anhidridą:
CH3CO (O) COCH2CH2CH2CH2CH2CH3
Kairėje esanti acetilo grupė yra iš acto rūgšties, o dešinėje - iš heptano rūgšties. Norėdami įvardinti šį anhidridą, turite nurodyti savo R grupes abėcėlės tvarka. Taigi, jo pavadinimas yra heptano acto rūgšties anhidridas.
Programos
Neorganiniai anhidridai turi begalinį panaudojimą: nuo medžiagų, keramikos, katalizatorių, cementų, elektrodų, trąšų ir kt. gyvų organizmų iškvepiamo anglies kiekio.
Jie yra išvykimo šaltinis - ta vieta, kur yra daugybė neorganinėje sintezėje naudojamų junginių. Vienas svarbiausių anhidridų yra anglies dioksidas, CO2. Jis kartu su vandeniu yra būtinas fotosintezei. Ir pramoniniu lygiu PK3 labai svarbu, nes atsakovas gauna sieros rūgštį.
Galbūt anhidridas, turintis daugiau paraiškų ir turintis (tol, kol yra gyvenimo), yra vienas iš fosforo rūgšties: adenozino trifosfato, geriau žinomas kaip ATP, esantis DNR ir "energinė valiuta" metabolizme.
Organiniai anhidridai
Rūgštiniai anhidridai reaguoja acilinimo būdu arba alkoholiui, kuris sudaro esterį, į aminą, kuris sukelia amidą arba aromatinį žiedą.
Kiekvienas iš šių junginių yra milijonai, o šimtai tūkstančių karboksirūgščių yra skirti anhidridui paruošti; todėl sintetinės galimybės drastiškai auga.
Taigi, vienas iš pagrindinių taikymo būdų yra įtraukti acilo grupę į junginį, pakeičiantį vieną iš jo struktūros atomų arba grupių.
Kiekvienas anhidridas atskirai turi savo taikymą, tačiau apskritai jie visi reaguoja panašiai. Dėl šios priežasties šie junginių tipai naudojami polimero struktūroms modifikuoti, kuriant naujus polimerus; ty kopolimerai, dervos, dangos ir tt.
Pavyzdžiui, acto anhidridas naudojamas visų OH celiuliozės grupių acetilinimui (apatinis vaizdas). Tokiu būdu kiekvienas H OH yra pakeistas acetilo grupe, COCH3.
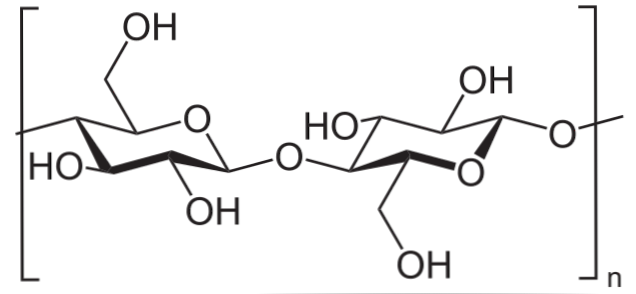
Tokiu būdu gaunamas celiuliozės acetato polimeras. Ta pati reakcija gali būti brėžiama su kitomis polimerinėmis struktūromis su NH grupėmis2, taip pat jautrūs acilinimui.
Šios acilinimo reakcijos taip pat yra naudingos vaistų, pvz., Aspirino (rūgšties) sintezei acetilosalicilas).
Pavyzdžiai
Kai kurie kiti organinių anhidridų pavyzdžiai yra baigti. Nors jų nebus paminėta, deguonies atomai gali būti pakeisti siera, suteikiant sierą arba net fosforo anhidridus..
-C6H5CO (O) COC6H5: benzenkarboksido anhidridas. C grupė6H5 reiškia benzeno žiedą. Jos hidrolizės metu susidaro dvi benzenkarboksirūgštys.
-HCO (O) COH: skruzdžių anhidridas. Jos hidrolizės metu susidaro dvi skruzdžių rūgštys.
- C6H5CO (O) COCH2CH3: benzenkarboksirūgšties anhidridas. Jos hidrolizė gamina benzoines ir propano rūgštis.
-C6H11CO (O) COC6H11: cikloheksankarboksirūgšties anhidridas. Skirtingai nuo aromatinių žiedų, jie yra prisotinti be dvigubų ryšių.
-CH3CH2CH2CO (O) COCH2CH3: butano propano rūgšties anhidridas.
Gintaro anhidridas

Čia mes turime kitą ciklinį, gautą iš gintaro rūgšties, dikarboksirūgšties. Atkreipkite dėmesį, kaip trys deguonies atomai išduoda šio tipo junginių cheminį pobūdį.
Maleino anhidridas yra labai panašus į gintaro anhidridą, skiriasi tuo, kad yra anglies junginių, sudarančių penkiakampį, dvigubas ryšys..
Glutaro anhidridas
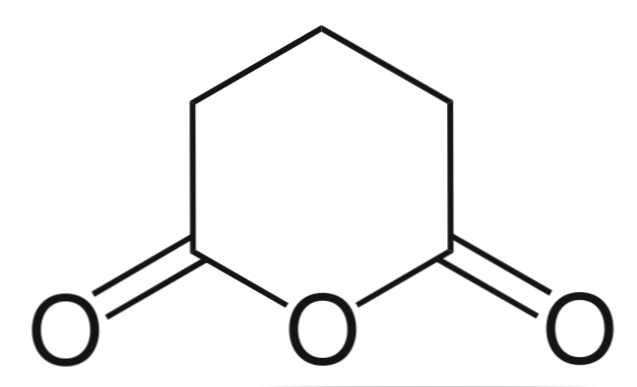
Galiausiai parodyta glutaro rūgšties anhidridas. Tai struktūriškai skiriasi nuo visų kitų, sudarant šešiakampį žiedą. Vėlgi, trys deguonies atomai išsiskiria struktūroje.
Kiti anhidridai, sudėtingesni, visada gali būti įrodomi trijų deguonies atomų, kurie yra labai arti vienas kito.
Nuorodos
- „Encyclopaedia Britannica“ redaktoriai. (2019). Anhidridas. Encryclopaedia Britannica. Gauta iš: britannica.com
- Helmenstine, Anne Marie, Ph.D. (2019 m. Sausio 8 d.). Rūgšties anhidrido apibrėžimas chemijoje. Gauta iš: thinkco.com
- Chemija LibreTexts. (s.f.). Anhidridai. Gauta iš: chem.libretexts.org
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organinė chemija. Aminai (10)th leidimas.). Wiley Plus.
- Carey F. (2008). Organinė chemija (Šeštasis leidimas). Mc Graw kalnas.
- Whitten, Davis, Peck & Stanley. (2008). Chemija (8-asis red.). Mokymosi mokymas.
- Morrison ir Boyd. (1987). Organinė chemija (Penktasis leidimas). Addison-Wesley Iberoamericana.
- Vikipedija. (2019). Organinių rūgščių anhidridas. Gauta iš: en.wikipedia.org


