Aukso oksido (III) (Au2O3) struktūra, savybės, nomenklatūra ir panaudojimas
The aukso oksidas (III) yra neorganinis junginys, kurio cheminė formulė yra Au2O3. Teoriškai galima tikėtis, kad jo pobūdis yra kovalentinis. Tačiau tam tikros joninės charakteristikos buvimas kietojoje medžiagoje negali būti visiškai pašalintas; arba tai, kas yra ta pati, daroma prielaida, kad nėra jokio pranešimo3+ šalia anijono O2-.
Gali atrodyti prieštaringa, kad auksas, kuris yra kilnus metalas, gali rūdyti. Esant normalioms sąlygoms, aukso gabalėliai (kaip ir paveiksle esančios žvaigždės) negali būti oksiduojami sąlyčio su deguonimi atmosferoje; tačiau, kai apšvitinama ultravioletine spinduliuote, kai yra ozono, OR3, vaizdas yra kitoks.

Jei aukso žvaigždės buvo laikomos šiomis sąlygomis, jos taps rausvai rudos, būdingos Au2O3.
Kiti šio oksido gavimo būdai būtų minėtų žvaigždžių cheminis apdorojimas; pavyzdžiui, paverčiant aukso masę į atitinkamą chloridą, AuCl3.
Po to į AuCl3, ir suformuotos kitos galimos aukso druskos, pridedama stipri bazinė terpė; ir su tuo jūs gausite hidratuotą oksidą arba hidroksidą, Au (OH)3. Galiausiai šis paskutinis junginys yra termiškai dehidratuotas, kad gautų Au2O3.
Indeksas
- 1 Aukso oksido struktūra (III)
- 1.1 Elektroniniai aspektai
- 1.2 Hidratai
- 2 Ypatybės
- 2.1 Fizinė išvaizda
- 2.2 Molekulinė masė
- 2.3 Tankis
- 2.4 Lydymosi temperatūra
- 2.5 Stabilumas
- 2.6 Tirpumas
- 3 Nomenklatūra
- 4 Naudojimas
- 4.1 Akinių dažymas
- 4.2 Auratų sintezė ir aukso užpildymas
- 4.3 Savarankiškai surinktų monolitų apdorojimas
- 5 Nuorodos
Aukso oksido struktūra (III)
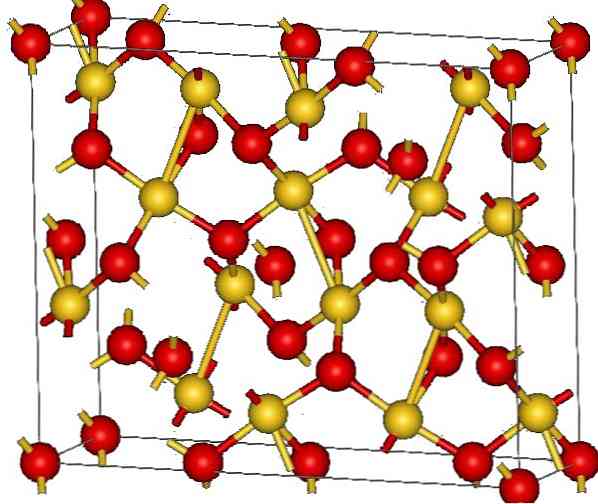
Viršutiniame paveikslėlyje parodyta aukso (III) oksido kristalinė struktūra. Parodyta aukso ir deguonies atomų išdėstymas kietoje medžiagoje, arba kaip neutralūs atomai (kovalentinė kieta medžiaga), arba kaip jonai (joninė kieta medžiaga). Bet kokiu atveju pakanka pašalinti ar įdėti Au-O nuorodas bet kuriuo atveju.
Pagal vaizdą daroma prielaida, kad vyrauja kovalentinis požymis (kuris būtų logiškas). Dėl šios priežasties atomai ir atributai yra rodomi atitinkamai su sferomis ir juostomis. Auksiniai rutuliai atitinka aukso atomus (AuIII-O) ir raudonų iki deguonies atomų.
Jei pažvelgsite atidžiai, pamatysite, kad yra AuO vienetų4, kuriuos jungia deguonies atomai. Kitas būdas vizualizuoti būtų laikyti, kad kiekviena Au3+ yra apsuptas keturių O2-; Žinoma, iš jonų perspektyvos.
Ši struktūra yra kristalinė, nes atomams pavedama laikytis to paties ilgojo nuotolio. Taigi, jos vieninga ląstelė atitinka romboedrinę kristalinę sistemą (tokia pati, kaip ir viršutiniame paveikslėlyje). Todėl visi Au2O3 galėtų būti pastatyta, jei visos tos vieneto ląstelės sferos būtų paskirstytos erdvėje.
Elektroniniai aspektai
Auksas yra pereinamasis metalas, ir tikimasi, kad jo 5d orbitos tiesiogiai sąveikauja su deguonies atomo 2p orbitomis. Šis jų orbitų sutapimas teoriškai turėtų generuoti laidumo juostas, kurios pakeistų Au2O3 kietajame puslaidininkyje.
Todėl tikra Au struktūra2O3 tai yra dar sudėtingesnė.
Hidratuoja
Aukso oksidas gali išlaikyti vandens molekules savo romboedriniuose kristaluose, kurie sukelia hidratus. Kai susidaro tokie hidratai, struktūra tampa amorfine, tai yra netvarkinga.
Tokių hidratų cheminė formulė gali būti bet kuri iš toliau išvardytų, kurie iš tikrųjų nėra aiškiai išaiškinti: Au2O3∙ zH2O (z = 1, 2, 3 ir tt), Au (OH)3, arba AuxOir(OH)z.
Formulė Au (OH)3 reiškia minėtų hidratų tikrosios kompozicijos supaprastinimą. Taip yra todėl, kad aukso hidroksido (III) viduje mokslininkai taip pat nustatė Au buvimą2O3; ir todėl yra prasminga ją apdoroti atskirai kaip „paprastą“ pereinamojo metalo hidroksidą.
Kita vertus, kietos medžiagos, kurių formulė AuxOir(OH)z galima tikėtis amorfinės struktūros; kadangi tai priklauso nuo koeficientų x, ir ir z, kurių variacijos sukeltų visų rūšių struktūrą, kuri vargu ar galėtų rodyti kristalinį modelį.
Savybės
Fizinė išvaizda
Tai rausvai rudos spalvos kieta medžiaga.
Molekulinė masė
441,93 g / mol.
Tankis
11,34 g / ml.
Lydymosi temperatūra
Jis lydosi ir skilsta 160 ° C temperatūroje. Todėl trūksta virimo taško, todėl šis oksidas niekada nepasiekia virimo temperatūros.
Stabilumas
Au2O3 jis yra termodinamiškai nestabilus, nes, kaip minėta pradžioje, auksas nėra linkęs oksiduotis normaliomis temperatūros sąlygomis. Taigi jis lengvai sumažinamas, kad vėl taptų kilnus auksas.
Kuo aukštesnė temperatūra, tuo greičiau reakcija, kuri vadinama terminiu skilimu. Taigi, Au2O3 160 ° C temperatūroje jis skaidosi, kad susidarytų metalinis auksas ir atleistų molekulinį deguonį:
2 Au2O3 => 4 Au + 3 O2
Labai panaši reakcija gali pasireikšti ir su kitais junginiais, skatinančiais minėtą redukciją. Kodėl mažinti? Kadangi auksas grįžta įgyti elektronų, kuriuos deguonis paėmė iš jo; tas pats, kas sako, kad praranda ryšį su deguonimi.
Tirpumas
Tai yra vandenyje netirpi kieta medžiaga. Tačiau jis yra tirpus druskos rūgštyje ir azoto rūgštyje, nes susidaro aukso chloridai ir nitratai.
Nomenklatūra
Aukso oksidas (III) yra pavadinimas, kuriam taikoma atsargų nomenklatūra. Kiti būdai paminėti tai yra:
-Tradicinė nomenklatūra: aurerio oksidas, nes valanda 3+ yra didžiausia auksui.
-Sisteminė nomenklatūra: dioro trioksidas.
Naudojimas
Akinių dažymas
Vienas iš svarbiausių jo panaudojimo būdų yra tam tikrų medžiagų, tokių kaip akiniai, raudonos spalvos suteikimas ir tam tikrų aukso atomų būdingų savybių suteikimas..
Auratų sintezė ir aukso užpildymas
Jei pridėta Au2O3 į terpę, kurioje jis tirpsta, ir esant metalams, auratai gali nusodinti po stiprios bazės; kuriuos sudaro AuO anijonai4- metalinių katijonų kompanijoje.
Be to, Au2O3 reaguoja su amoniaku, kad susidarytų aukso užpildas, Au2O3(NH3)4. Jo pavadinimas kyla iš to, kad jis yra labai sprogus.
Savarankiškai surinktų monolitų apdorojimas
Ant aukso ir jo oksido tam tikri junginiai, tokie kaip dialkildisulfidai, RSSR, nėra adsorbuojami taip pat. Kai atsiranda ši adsorbcija, spontaniškai susidaro Au-S jungtis, kur sieros atomas turi ir apibrėžia minėto paviršiaus chemines savybes, priklausomai nuo funkcinės grupės, prie kurios jis yra prijungtas..
RSSR negali adsorbuoti Au2O3, bet ant metalinio aukso. Todėl, jei aukso paviršius ir oksidacijos laipsnis yra modifikuoti, taip pat Au dalelių ar sluoksnių dydis.2O3, gali būti sukurtas heterogeniškesnis paviršius.
Šis paviršius Au2O3-AuSR sąveikauja su tam tikrų elektroninių prietaisų metaliniais oksidais, taip kurdamas ateityje pažangesnius paviršius.
Nuorodos
- Vikipedija. (2018). Aukso (III) oksidas. Gauta iš: en.wikipedia.org
- Cheminė formuluotė (2018). Aukso oksidas (III). Susigrąžinta iš: Formacionquimica.com
- D. Michaud. (2016 m. Spalio 24 d.). Aukso oksidai. 911 Metalurgas. Gauta iš: 911metallurgist.com
- Shi, R. Asahi ir C. Stampfl. (2007). Aukso oksidų savybės2O3 ir Au2O: Pirmosios principų tyrimas. Amerikos fizinė draugija.
- Cook, Kevin M. (2013). Aukso oksidas kaip maskavimo sluoksnis regioselektyviai paviršiaus chemijai. Disertacijos ir disertacijos. 1460 dokumentas.


