Kalcio oksido (CaO) struktūra, savybės ir naudojimo būdai
The kalcio oksidas (CaO) yra neorganinis junginys, kurio sudėtyje yra kalcio ir deguonies jonų pavidalu (negali būti painiojamas su kalcio peroksidu, CaO).2). Visame pasaulyje žinoma kaip kalkė - žodis, kuris žymi bet kokį neorganinį junginį, kuriame yra karbonatų, kalcio oksidų ir hidroksidų, taip pat kitus metalus, tokius kaip silicis, aliuminis ir geležis..
Šis oksidas (arba kalkės) taip pat vadinamas bendradar- biais kaip kalkės arba gesintos kalkės, priklausomai nuo to, ar jis yra hidratuotas, ar ne. Kalkės yra kalcio oksidas, o hidratuotas kalkės. Savo ruožtu, kalkakmenis (kalkių arba sukietėjusių kalkių) iš tiesų yra nuosėdų uoliena, daugiausia sudaryta iš kalcio karbonato (CaCO).3).

Tai vienas didžiausių natūralių kalcio šaltinių ir yra žaliava kalcio oksido gamybai. Kaip gaminamas šis oksidas? Karbonatai yra jautrūs terminiam skilimui; kalcio karbonatų kaitinimas esant aukštesnei nei 825 ° C temperatūrai, todėl susidaro kalkės ir anglies dioksidas.
Anksčiau pateiktas teiginys gali būti aprašytas taip: CaCO3(s) → CaO (s) + CO2(g) Kadangi žemės plutos yra gausios kalkakmeniu ir kalcitu, o vandenynuose ir paplūdimiuose gausu jūros kriauklių (žaliavų kalcio oksido gamybai), kalcio oksidas yra palyginti pigus reagentas.
Indeksas
- 1 Formulė
- 2 Struktūra
- 3 Ypatybės
- 3.1 Tirpumas
- 4 Naudojimas
- 4.1. Kaip skiedinys
- 4.2 Stiklų gamyboje
- 4.3 Kasyba
- 4.4 Kaip silikato valiklis
- 5 Kalcio oksido nanodalelės
- 6 Nuorodos
Formulė
Kalcio oksido cheminė formulė yra CaO, kuriame kalcis yra toks pat kaip rūgšties jonas (elektronų priėmėjas) Ca2+, ir deguonis kaip bazinis jonas (elektronų donoras) ARBA2--.
Kodėl kalcio turi +2 mokestį? Kadangi kalcis priklauso periodinės lentelės 2 grupei (p. Becambara), ir turi tik du valentų elektronus, galinčius sudaryti ryšius, kurie duoda deguonies atomą..
Struktūra
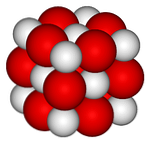
Viršutiniame vaizde yra kalcio oksido kristalinė struktūra (gem-salt type). Dideli raudoni rutuliai atitinka Ca jonus2+ ir baltieji rutuliai prie jonų O2-.
Šiame kubiniame kristalų išdėstyme kiekviena jonų Ca2+ yra apsuptas šešių jonų O2-, okliedinės skylės, tarp kurių yra dideli jonai.
Ši struktūra išreiškia maksimalų šio oksido jonų pobūdį, nors didelis spindulių skirtumas (raudonasis rutulys yra didesnis nei baltas) suteikia silpnesnę kristalinę tinklinę energiją, palyginti su MgO.
Savybės
Fiziškai tai yra kristalinė balta kieta medžiaga, bekvapė ir su stipria elektrostatine sąveika, kuri yra atsakinga už aukštus lydymosi taškus (2572 ° C) ir verdančią (2850 ° C). Be to, jo molekulinė masė yra 55,958 g / mol ir įdomi termoliuminescencinė savybė.
Tai reiškia, kad liepsnos paveiktas kalcio oksido gabalas gali švytėti intensyviai balta šviesa, žinoma anglų kalba su pavadinimu šviesa, arba ispanų kalba, kalcio šviesa. Ca jonai2+, liečiant ugnį, jie sukelia rausvą liepsną, kaip parodyta šiame paveikslėlyje.

Tirpumas
CaO yra bazinis oksidas, turintis stiprų afinitetą vandeniui tiek, kiek jis sugeria drėgmę (tai yra higroskopinė kieta medžiaga), nedelsiant reaguojant į gesintą kalkę arba kalcio hidroksidą:
CaO (s) + H2O (l) => Ca (OH)2(-ai)
Ši reakcija yra egzoterminė (išskiria šilumą) dėl stipresnės sąveikos ir stabilesnės kristalinės grotelės susidarymo. Tačiau, jeigu Ca (OH) yra kaitinama, reakcija yra grįžtama2, dehidratuoti ir apšviesti gesintą kalkę; tada kalkė „atgimsta“.
Gautas tirpalas yra labai paprastas, o jei jis yra prisotintas kalcio oksidu, jis pasiekia 12,8 pH.
Taip pat jis tirpsta glicerolyje ir rūgščių bei cukraus tirpaluose. Kadangi tai yra bazinis oksidas, jis natūraliai veikia veiksmingai su rūgšties oksidais (SiO2, Al2O3 ir tikėjimas2O3, pvz., tirpsta jų skystose fazėse. Kita vertus, jis netirpsta alkoholiuose ir organiniuose tirpikliuose.
Naudojimas
CaO turi daug pramoninės paskirties, taip pat acetileno sintezės (CH≡CH), išgaunant fosfatus iš nuotekų ir reaguojant su sieros dioksidu iš dujinių atliekų..
Kiti kalcio oksido naudojimo būdai aprašyti toliau:
Kaip skiedinys
Jei kalcio oksidas yra sumaišytas su smėliu (SiO2) ir vanduo, pyragai su smėliu ir lėtai reaguoja su vandeniu, kad susidarytų gesintos kalkės. Savo ruožtu, CO2 oro ištirpsta vandenyje ir reaguoja su druska, kad susidarytų kalcio karbonatas:
Ca (OH)2s) CO2(g) => CaCO3(s) + H2O (l)
CaCO3 Jis yra labiau atsparus ir kietesnis junginys nei CaO, todėl skiedinys (ankstesnis mišinys) sukietėja ir tvirtina plytas, blokus ar keramiką tarp jų arba norimo paviršiaus..
Gaminant akinius
Pagrindinė žaliava stiklo gamybai yra silicio oksidai, kurie yra sumaišyti su kalkėmis, natrio karbonatu (Na2CO3) ir kitų priedų, kurie vėliau apšildomi, todėl susidaro stiklinė kieta medžiaga. Vėliau ši kieta medžiaga kaitinama ir išpurškiama bet kokiais skaičiais.
Kasyba
Dėl vandenilio surišimo (O-H-O) sąveikos sluoksniuotos kalkės užima didesnį tūrį nei kalkės. Ši ypatybė naudojama uolienų pertraukimui iš vidaus.
Tai pasiekiama užpildant juos kompaktišku kalkių ir vandens mišiniu, kuris yra užplombuotas, kad sutelktų savo šilumą ir ekspansyviąją galią uoloje..
Kaip silikato valiklis
CaO yra sujungtas su silikatais, kad susidarytų koalescentinis skystis, kuris ekstrahuojamas iš tam tikro produkto žaliavos.
Pavyzdžiui, geležies rūdos yra metalo geležies ir plieno gamybos žaliava. Šiuose mineraluose yra silikatų, kurie yra nepageidaujamos priemaišos procesui ir yra pašalintos naudojant tik aprašytą metodą.
Kalcio oksido nanodalelės
Kalcio oksidas gali būti sintezuojamas kaip nanodalelės, keičiant kalcio nitrato (Ca (NO)) koncentracijas3)2) ir natrio hidroksido (NaOH) tirpale.
Šios dalelės yra sferinės, bazinės (taip pat ir makroskopinės kietosios medžiagos) ir turi daug paviršiaus ploto. Todėl šios savybės yra naudingos kataliziniams procesams. Kuris? Tyrimai šiuo metu atsako į šį klausimą.
Šios nanodalelės buvo panaudotos pakaitinių organinių junginių, gautų iš piridinų, sintezei formuojant naujus vaistus, kad būtų atliekamos cheminės transformacijos, pvz., Dirbtinė fotosintezė, vandens valymui iš sunkiųjų ir kenksmingų metalų, ir fotokatalitiniai agentai.
Nanodalelės gali būti sintezuojamos ant biologinės paramos, pavyzdžiui, papajos ir žaliosios arbatos lapai, naudojami kaip antibakterinis agentas.
Nuorodos
- scifun.org (2018 m.). Kalkės: kalcio oksidas. Gauta 2018 m. Kovo 30 d., Iš: scifun.org.
- Vikipedija. (2018). Kalcio oksidas. Gauta 2018 m. Kovo 30 d. Iš: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Žalioji kalcio oksido nanodalelių ir jos panaudojimo sintezė. Inžinerinių tyrimų ir taikymo žurnalas. ISSN: 2248-9622, 6 tomas, 10 leidimas, (-1 dalis), p.
- J. Safaei-Ghomi ir kt. (2013). Kalcio oksido nanodalelės katalizavo vienos pakopos daugiakomponentę labai pakeistų piridinų sintezę vandeninėje etanolio terpėje Scientia Iranica, operacijos C: chemija ir chemijos inžinerija 20 549-554.
- PubChem. (2018). Kalcio oksidas. Gauta 2018 m. Kovo 30 d., Iš: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Neorganinė chemija Į 2 grupės elementai. (ketvirtasis leidimas, 280 psl.). Mc Graw kalnas.


