Juostų modelio ir pavyzdžių teorija
The juostos teorija yra tai, kuri apibrėžia elektroninę kietosios medžiagos struktūrą. Jis gali būti taikomas bet kokio tipo kietosioms medžiagoms, tačiau jis yra metalų, kuriuose atsispindi didžiausios sėkmės. Pagal šią teoriją metalo jungtis atsiranda dėl elektrostatinio pritraukimo tarp teigiamai įkrautų jonų ir mobiliųjų elektronų kristale..
Todėl metalinis kristalas turi „elektronų jūrą“, kuri gali paaiškinti jo fizines savybes. Apatinis vaizdas iliustruoja metalinę nuorodą. Elektronų violetiniai taškai yra perkeliami į jūrą, kuri apgaubia teigiamai įkrautus metalo atomus.

"Elektronų jūra" formuojama iš kiekvieno metalo atomo individualių įnašų. Šie indėliai yra atominės orbitos. Metalo konstrukcijos paprastai yra kompaktiškos; kuo kompaktiškesni jie yra, tuo didesnė jų atomų sąveika.
Dėl to jų atominės orbitos sutampa, kad generuotų labai siauras molekulines orbitales. Tuomet elektronų jūra yra tik didelis molekulinių orbitonų rinkinys su skirtingais energijos intervalais. Šių energijų diapazonas sudaro tai, kas žinoma kaip energijos juostos.
Šios juostos yra bet kuriame kristalo regione, todėl jis laikomas visuma, ir iš ten ateina šios teorijos apibrėžimas.
Indeksas
- 1 Energijos juostų modelis
- 1.1 Fermio lygis
- 2 Puslaidininkiai
- 2.1 Vidiniai ir išoriniai puslaidininkiai
- 3 Taikomosios juostos teorijos pavyzdžiai
- 4 Nuorodos
Energijos juostų modelis

Kai metalo atomo orbitalis sąveikauja su jo kaimyno orbitu (N = 2), susidaro dvi molekulinės orbitos: viena iš jungties (žalios juostos) ir viena anti-link (tamsiai raudona juosta).
Jei N = 3, dabar susidaro trys molekulinės orbitos, iš kurių vidutinis (juoda juosta) yra neprivalomas. Jei N = 4, yra suformuotos keturios orbitos, o tas, kuriam būdingas didžiausias privalomasis požymis, ir vienas, turintis didžiausią užšalimo charakterį..
Molekulinėms orbitoms prieinamos energijos diapazonas plečiasi, nes kristalų metaliniai atomai yra jų orbitos. Tai taip pat sumažina energijos erdvę tarp orbitų iki taško, kad jie kondensuotų juostoje.
Ši orbitačių grupė turi mažai energijos (žalios ir geltonos spalvos) ir didelę energiją (oranžinės ir raudonos spalvos). Jų energetiniai kraštutinumai turi mažą tankį; tačiau dauguma molekulinių orbitalių (baltos juostelės) yra sutelktos centre.
Tai reiškia, kad elektronai „veikia greičiau“ per juostos centrą nei jų galuose.
Fermio lygis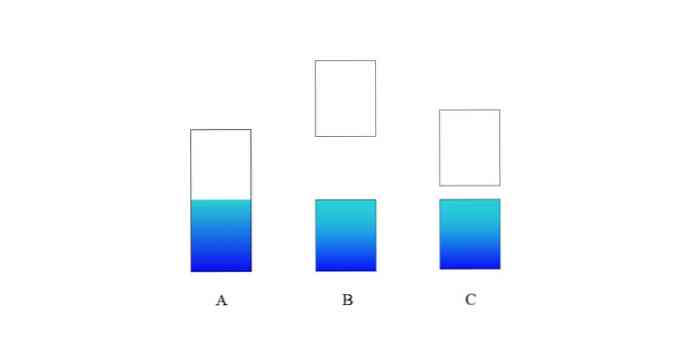
Tai didžiausia energijos būsena, užimta elektronų, esančių kietoje, absoliučioje nulio temperatūroje (T = 0 K).
Sukūrus juostą, elektronai pradeda užimti visas jų molekulines orbitales. Jei metalas turi vieną valentinį elektroną (-us)1) visi jo kristalų elektronai užims pusę juostos.
Kita nepanaudota pusė vadinama vairavimo juosta, o elektronų pilna juosta vadinama valentine juosta.
Viršutiniame vaizde A yra tipinė valentinė juosta (mėlyna) ir laidumo juosta (balta) metalui. Mėlyna sienos linija rodo Fermio lygį.
Kadangi metalai taip pat turi p-orbitų, jie kartu suformuoja p-juostą (balta).
Metalų atveju s ir p juostos yra labai arti energijos. Tai leidžia jų persidengimą, skatinant elektronus nuo valentinės juostos iki laidumo juostos. Taip atsitinka net esant temperatūrai, mažai virš 0 K.
Pereinamųjų metalų ir nuo 4-ojo laikotarpio žemyn taip pat galima suformuoti.
Fermi lygis laidumo juostos atžvilgiu yra labai svarbus nustatant elektrines savybes.
Pavyzdžiui, metalo Z, kurio Fermi lygis yra labai arti laidumo juostos (artimiausia tuščia juosta energijoje), turi didesnį elektros laidumą nei X metalas, kuriame jo Fermi lygis yra toli nuo tos juostos..
Puslaidininkiai
Tada elektros laidumas susideda iš elektronų migracijos iš valentinės juostos į laidumo juostą.
Jei energijos tarpas tarp abiejų juostų yra labai didelis, mes turime izoliacinę kietą medžiagą (kaip ir B). Kita vertus, jei ši spraga yra palyginti maža, kietoji medžiaga yra puslaidininkė (C atveju)..
Susidūrus su temperatūros didėjimu, valentinės juostos elektronai gauna pakankamai energijos, kad galėtų pereiti prie laidumo juostos. Tai sukelia elektros srovę.
Tiesą sakant, tai yra kietųjų medžiagų arba puslaidininkinių medžiagų kokybė: kambario temperatūroje jie yra izoliatoriai, tačiau esant aukštai temperatūrai jie yra laidininkai..
Vidiniai ir išoriniai puslaidininkiai

Vidiniai laidininkai yra tie, kuriuose energijos atotrūkis tarp valentinės juostos ir laidumo juostos yra pakankamai mažas, kad šiluminė energija leidžia elektronams praeiti..
Kita vertus, išoriniai laidininkai keičia savo elektronines konstrukcijas po dopingo su priemaišomis, kurios padidina jų elektrinį laidumą. Ši priemaiša gali būti kitas metalas arba nemetalinis elementas.
Jei priemaiša turi daugiau valentinių elektronų, ji gali suteikti donoro juostą, kuri tarnauja kaip tiltas juostos elektronams kirsti į laidumo juostą. Šios kietosios medžiagos yra n tipo puslaidininkiai. Čia n pavadinimas atsiranda iš „neigiamo“.
Viršutiniame paveikslėlyje donoro juosta yra parodyta mėlynos spalvos bloke, žemiau vairavimo juostos (n tipas).
Kita vertus, jei priemaiša turi mažiau valentinių elektronų, ji suteikia akceptoriaus juostą, kuri sutrumpina energijos atotrūkį tarp valentinės juostos ir vairavimo juostos..
Elektronai pirmiausia migruoja į šią juostą, paliekant „teigiamas skyles“, kurios juda priešinga kryptimi.
Kadangi šie teigiami tarpai žymi elektronų judėjimą, kietoji medžiaga arba medžiaga yra p tipo puslaidininkis..
Taikomosios juostos teorijos pavyzdžiai
- Paaiškinkite, kodėl metalai yra ryškūs: jų mobilieji elektronai gali sugerti spinduliuotę įvairiuose bangos ilgiuose, kai jie pereina į aukštesnį energijos lygį. Tada jie skleidžia šviesą, sugrįždami į žemesnius vairavimo juostos lygius.
- Kristalinis silicis yra svarbiausia puslaidininkinė medžiaga. Jei silicio dalis yra sujungta su 13 grupės elemento pėdsakais (B, Al, Ga, In, Tl), ji tampa p-tipo puslaidininkiu. Kadangi, jei jis yra sujungtas su 15 grupės elementu (N, P, As, Sb, Bi), jis tampa n tipo puslaidininkiu.
- Šviesos diodas (LED) yra jungtinis puslaidininkis p-n. Ką reiškia? Kad medžiaga turi abiejų puslaidininkių tipus, tiek n, tiek p. Elektronai migruoja iš n tipo puslaidininkio laidumo juostos prie p tipo puslaidininkio valentinės juostos.
Nuorodos
- Whitten, Davis, Peck & Stanley. Chemija (8-asis red.). CENGAGE mokymasis, p. 486-490.
- Shiver & Atkins. (2008). Neorganinė chemija (Ketvirtas leidimas., P. 103-107, 633-635). Mc Graw kalnas.
- Laivas C. R. (2016). Kietųjų dalelių juostos teorija. Gauta 2018 m. Balandžio 28 d., Iš: hyperphysics.phy-astr.gsu.edu
- Steve Kornic (2011). Eidami iš obligacijų į grupes iš chemiko požiūrio. Gauta 2018 m. Balandžio 28 d., Iš: chembio.uoguelph.ca
- Vikipedija. (2018). Išorinis puslaidininkis. Gauta 2018 m. Balandžio 28 d., Iš: en.wikipedia.org
- BYJU. (2018). Metalų juostos teorija. Gauta 2018 m. Balandžio 28 d., Nuo: byjus.com



