Amonio hidroksido struktūra, savybės, nomenklatūra, panaudojimas
The amonio hidroksido yra NH molekulinės formulės junginys4OH arba H5NEGALIMA ištirpinant amoniako dujas (NH3) vandenyje. Dėl šios priežasties jis gauna amoniako vandens ar skysto amoniako pavadinimus.
Tai bespalvis skystis, turintis labai intensyvų ir aštrią kvapą, kuris nėra izoliuojantis. Šios savybės yra tiesiogiai susijusios su NH koncentracija3 ištirpintas vandenyje; koncentracija, kuri, tiesą sakant, yra dujos, gali apimti didžiulį jo kiekį, ištirpintą mažame vandens kiekyje.
Labai maža šių vandeninių tirpalų dalis susideda iš NH katijonų4+ ir OH anijonai-. Kita vertus, labai praskiestuose tirpaluose arba užšaldytose kietose medžiagose labai žemoje temperatūroje amoniaką galima rasti hidratų pavidalu, pavyzdžiui: NH3∙ H2O, 2NH3∙ H2O ir NH3∙ 2H2O.
Kaip įdomus faktas, Jupiterio debesys susidaro praskiestuose amonio hidroksido tirpaluose. Tačiau „Galileo“ kosmoso zondas nepavyko rasti vandens planetos debesyse, o tai būtų tikimasi žinant, kad žinomas amonio hidroksido susidarymas; tai yra NH kristalai4OH visiškai bevandenis.
Amonio jonas (NH4+) gaminamas inkstų kanalėlių liumenoje amoniako ir vandenilio sąveika, kurią išskiria inkstų kanalėlių ląstelės. Taip pat, amonio susidaro inkstų kanalėlių ląstelėse glutamino transformavimo į glutamatą procese ir, savo ruožtu, glutamato pavertimu α-ketoglutaratu..
Amoniakas gaminamas pramoniniu būdu pagal Haber-Bosch metodą, kuriame reaguoja azoto ir vandenilio dujos; naudojant katalizatorių naudojant geležies joną, aliuminio oksidą ir kalio oksidą. Reakcija atliekama esant aukštam slėgiui (150–300 atmosferų) ir aukštai temperatūrai (400–500 ° C), kurių išeiga yra 10–20%..
Reakcijos metu susidaro amoniakas, kuris oksidavus gamina nitritus ir nitratus. Tai labai svarbu norint gauti azoto rūgštį ir trąšas, pvz., Amonio nitratą.
Indeksas
- 1 Cheminė struktūra
- 1.1 Amoniakinis ledas
- 2 Fizinės ir cheminės savybės
- 2.1 Molekulinė formulė
- 2.2 Molekulinė masė
- 2.3 Išvaizda
- 2.4 Koncentracija
- 2.5 Kvapas
- 2.6 Skonis
- 2.7 Ribinė vertė
- 2.8 Virimo temperatūra
- 2.9 Tirpumas
- 2.10 Tirpumas vandenyje
- 2.11 Tankis
- 2.12 Garų tankis
- 2.13 Garų slėgis
- 2.14 Korozinis poveikis
- 2,15 pH
- 2.16 Disociacijos konstanta
- 3 Nomenklatūra
- 4 Tirpumas
- 5 Rizika
- 5.1 Reaktingumas
- 6 Naudojimas
- 6.1 Maistas
- 6.2 Terapija
- 6.3 Pramoniniai ir įvairūs
- 6.4 Žemės ūkyje
- 7 Nuorodos
Cheminė struktūra
Kaip nurodyta jo apibrėžime, amonio hidroksidas susideda iš vandeninio amoniako dujų tirpalo. Todėl skystyje nėra apibrėžtos struktūros, išskyrus atsitiktinę NH jonų struktūrą4+ ir OH- tirpina vandens molekulės.
Amonio ir hidroksilo jonai yra amoniako hidrolizės pusiausvyros produktai, todėl yra įprasta, kad šie tirpalai pasižymi aštriu kvapu:
NH3(g) + H2O (l) <=> NH4+(ac) + OH-(ac)
Pagal cheminę lygtį didelio vandens koncentracijos sumažėjimo pusiausvyra nukreipta į daugiau amoniako susidarymą; ty amonio hidroksido kaitinimas, amoniako garai bus išleisti.
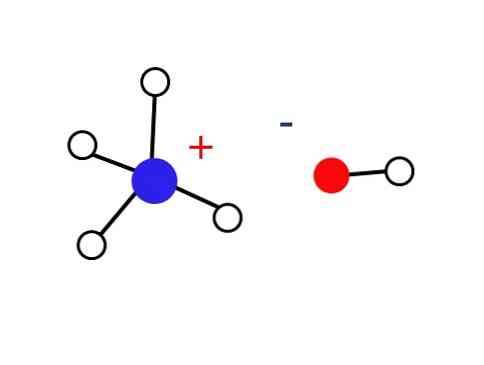
Dėl šios priežasties NH jonai4+ ir OH- jie nesugeba formuoti kristalų sausumos sąlygomis, o tai reiškia, kad kieta bazė NH4OH nėra.
Ši kieta medžiaga turi būti sudaryta tik iš jonų, veikiančių elektrostatiniu būdu (kaip parodyta paveikslėlyje)..
Amoniakinis ledas
Tačiau esant žemesnei nei 0 ° C temperatūrai ir apsupti milžiniško spaudimo, pavyzdžiui, ledinių mėnulių branduoliuose, amoniako ir vandens užšalimo. Tokiu būdu jie kristalizuojasi kietame mišinyje su įvairiomis stechiometrinėmis proporcijomis, tai yra paprasčiausias NH3∙ H2O: amoniako monohidratas.
NH3∙ H2O ir NH3∙ 2H2Arba jie yra amoniakinis ledas, nes kietąja medžiaga yra kristalinis vandens molekulių ir amoniako išdėstymas, sujungtas vandenilio jungtimis.
Atsižvelgiant į T ir P pokyčius, remiantis skaičiavimo tyrimais, imituojančiais visus fizinius kintamuosius ir jų poveikį šiems ledams, vyksta NH fazės perėjimas.3∙ nH2Arba NH fazei4OH.
Todėl tik šiomis ekstremaliomis sąlygomis NH4OH gali egzistuoti kaip protonacijos produktas lede tarp NH3 ir H2O:
NH3(s) + H2O (s) <=> NH4OH (-ai)
Atkreipkite dėmesį, kad šį kartą, skirtingai nei amoniako hidrolizė, susijusios rūšys yra kietos. Amoniakinis ledas, kuris tampa sūrus, neatleidžiant amoniako.
Fizinės ir cheminės savybės
Molekulinė formulė
NH4OH arba H5NE
Molekulinė masė
35,046 g / mol
Išvaizda
Tai bespalvis skystis.
Koncentracija
Iki 30% (NH jonams4+ ir OH-).
Kvapas
Labai stiprus ir ryškus.
Skonis
Acre.
Ribinė vertė
34 ppm nespecifiniam aptikimui.
Virimo temperatūra
38 ° C (25%).
Tirpumas
Jis yra tik vandeniniame tirpale.
Tirpumas vandenyje
Maišoma neribotomis dalimis.
Tankis
0,90 g / cm3 25 ° C temperatūroje.
Garų tankis
Santykis su oru, paimtu kaip vienetas: 0.6. Tai yra mažiau tankus nei oras. Tačiau logiška, kad nurodyta vertė reiškia amoniaką kaip dujas, o ne jo vandeninius tirpalus arba NH4OH.
Garų slėgis
2.160 mmHg esant 25 ° C temperatūrai.
Ėsdinantis poveikis
Jis gali ištirpinti cinką ir varį.
pH
11.6 (1 N tirpalas); 11.1 (0,1 tirpalas N) ir 10,6 (0,01 N tirpalas).
Disociacijos konstanta
pKb = 4,767; Kb = 1,71 x 10-5 20 ° C temperatūroje
pKb = 4,751; Kb = 1,774 x 10-5 esant 25 ° C temperatūrai.
Temperatūros padidėjimas beveik nepastebimai padidina amonio hidroksido bazę.
Nomenklatūra
Kokie yra bendri ir oficialūs pavadinimai, kuriuos NH gauna?4OH? Pagal tai, ką nustato IUPAC, jo pavadinimas yra amonio hidroksidas, nes jame yra hidroksilo anijono.
Amoniumas, kurį sudaro apkrova +1, yra monovalentinis, priežastis, kodėl naudojama nomenklatūra Atsargos, kurios pavadinamos kaip: amonio hidroksidas (I).
Nors terminas „amonio hidroksidas“ yra techniškai neteisingas, nes junginys nėra izoliuotas (bent jau ne žemėje, kaip išsamiai paaiškinta pirmame skyriuje)..
Be to, amonio hidroksidas gauna amoniako vandens ir skysto amoniako pavadinimus.
Tirpumas
NH4OH, nes sausumos sąlygomis nėra druskos, negalima įvertinti, kaip tirpus jis yra skirtinguose tirpikliuose.
Tačiau galima tikėtis, kad jis bus labai tirpus vandenyje, nes jo ištirpinimas atpalaiduoja milžiniškus NH kiekius3. Teoriškai tai būtų nuostabus būdas laikyti ir transportuoti amoniaką.
Kituose tirpikliuose, galinčiuose priimti vandenilio jungtis, pavyzdžiui, alkoholius ir aminus, galima tikėtis, kad jis taip pat labai tirpsta jose. Čia NH katijonas4+ yra vandenilio tiltų donorė ir OH- jis veikia kaip abu.
Tokių sąveikos su metanoliu pavyzdžiai būtų: H3N+-H - OHCH3 ir HO- - HOCH3 (OHCH3 rodo, kad deguonis gauna vandenilio jungtį, o ne, kad metilo grupė yra susieta su H).
Rizika
-Susilietus su akimis, sudirginimas gali sukelti akių pažeidimus.
-Jis yra ėsdinantis. Todėl, esant sąlyčiui su oda, gali atsirasti dirginimas ir esant didelei reagento koncentracijai, atsiranda odos nudegimų. Pakartotinis amonio hidroksido sąlytis su oda gali sukelti jo sausumą, niežulį ir paraudimą (dermatitą)..
-Įkvėpus amonio hidroksido purškimo gali atsirasti ūminis kvėpavimo takų dirginimas, kuriam būdingas uždusimas, kosulys ar dusulys. Ilgalaikis arba kartotinis medžiagos poveikis gali sukelti pasikartojančias bronchų infekcijas. Be to, amonio hidroksido įkvėpimas gali sukelti plaučių dirginimą.
-Didelės amonio hidroksido koncentracijos poveikis gali būti neatidėliotinas, nes gali atsirasti skysčių kaupimasis plaučiuose (plaučių edema)..
-25 ppm koncentracija buvo laikoma poveikio ribine verte per 8 valandų darbo laiką aplinkoje, kurioje darbuotojas susiduria su kenksmingu amonio hidroksido poveikiu..
Reaktingumas
-Be to, dėl amonio hidroksido poveikio galimo žalos sveikatai yra ir kitų atsargumo priemonių, į kurias reikia atsižvelgti dirbant su medžiaga.
-Amonio hidroksidas gali reaguoti su daugeliu metalų, pavyzdžiui, sidabro, vario, švino ir cinko. Jis taip pat reaguoja su šių metalų druskomis ir sudaro sprogius junginius ir išskiria vandenilio dujas; kuri, savo ruožtu, yra degi ir sprogi.
-Jis gali smarkiai reaguoti su stipriomis rūgštimis, pavyzdžiui: druskos rūgštimi, sieros rūgštimi ir azoto rūgštimi. Panašiai jis taip pat reaguoja su dimetilo sulfatu ir halogenais.
-Reaguoja su stipriomis bazėmis, pvz., Natrio hidroksidu ir kalio hidroksidu, gamindamas dujinį amoniaką. Tai galima patikrinti, jei pastebima tirpalo pusiausvyra, į kurią įpilama OH jonų- balansas perkeliamas į NH formavimą3.
-Vario ir aliuminio metalai, taip pat kiti cinkuoti metalai neturėtų būti naudojami apdorojant amonio hidroksidą dėl jų korozijos..
Naudojimas
Maistas
-Jis naudojamas kaip priedas daugelyje maisto produktų, kuriuose jis veikia kaip rauginamasis agentas, pH kontrolė ir maisto paviršiaus apdailos agentas..
-Maisto produktų, kuriuose naudojamas amonio hidroksidas, sąrašas yra platus ir apima kepinius, sūrius, šokoladus, saldainius ir pudingus..
-Maisto perdirbimui FDA amonio hidroksidą klasifikuoja kaip saugią medžiagą, jei laikomasi nustatytų standartų.
-Mėsos produktuose jis naudojamas kaip antimikrobinis agentas, gebantis pašalinti bakterijas, pvz., E. coli, sumažindamas jį iki nenustatyto lygio. Bakterijos randamos galvijų žarnyne, prisitaikiusios prie rūgštinės aplinkos. Amonio hidroksidas, reguliuodamas pH, trukdo bakterijų augimui.
Terapija
-Amonio hidroksidas turi keletą gydymo būdų, įskaitant:
-10% tirpalas naudojamas kaip kvėpavimo refleksas
-Išoriškai jis naudojamas ant odos vabzdžių įkandimų ir įkandimų gydymui. Jis veikia virškinimo sistemą kaip antacidinį ir karmininį, ty padeda pašalinti dujas.
Be to, jis vartojamas kaip aktualios ir lėtinės raumenų ir kaulų skausmo aktualios priemonės. Dėl gausaus amonio hidroksido poveikio yra padidėjęs kraujo tekėjimas, paraudimas ir dirginimas..
Pramoniniai ir įvairūs
-Jis mažina NOx (labai reaktyvios dujos, pvz., Azoto oksidas (NO) ir azoto dioksidas (NO))2)) kamino išmetamųjų teršalų ir išmetamų NOx kiekio sumažinimas.
-Jis naudojamas kaip plastifikatorius; Dažų priedas ir paviršių apdorojimas.
-Jis padidina plaukų poringumą, leidžiančią dažų pigmentams įsiskverbti į didesnį paviršių, o tai užtikrina geresnį apdailą.
-Amonio hidroksidas naudojamas kaip antimikrobinis agentas nuotekų valymui. Be to, ji įsikiša į chloramino sintezę. Ši medžiaga atitinka panašią į chlorą funkciją valant baseino vandenį, turintį pranašumą, kad jis yra mažiau toksiškas.
-Jis naudojamas kaip korozijos inhibitorius naftos valymo procese.
-Jis naudojamas kaip valymo priemonė įvairiuose pramoniniuose ir komerciniuose produktuose, naudojamuose ant kelių paviršių, įskaitant: nerūdijančio plieno, porceliano, stiklo ir orkaitės.
-Be to, jis naudojamas ploviklių, muilų, vaistų ir dažų gamyboje.
Žemės ūkyje
Nors amonio hidroksidas tiesiogiai nepateikiamas kaip trąšos, ši funkcija atliekama. Amoniakas gaminamas iš atmosferos azoto Haber-Bosch metodu ir transportuojamas šaldytuve žemiau virimo temperatūros (-33 ° C) iki jo naudojimo vietų.
Slėginis amoniakas yra įleidžiamas garais į dirvą, kur jis nedelsdamas reaguoja su edafiniu vandeniu ir patenka į amonio formą (NH4+), kuris išlieka dirvožemio katijonų mainų vietose. Be to, susidaro amonio hidroksidas. Šie junginiai yra azoto šaltinis.
Kartu su fosforu ir kaliu azotas sudaro pagrindinių augalų maistinių medžiagų, būtinų jo augimui, triadą.
Nuorodos
- Ganong, W. F. (2002). 19-asis leidimas. Redakcinis šiuolaikinis vadovas.
- A. D. Fortes, J. P. Brodholt, I. G. Wood ir L. Vocadlo. (2001). Ab initio amoniako monohidrato (NH) modeliavimas3∙ H2O) ir amonio hidroksido (NH4OH). Amerikos fizikos institutas. J. Chem. Phys., 115, Nr. 15, 15.
- Helmenstine, Anne Marie, Ph.D. (2017 m. Vasario 6 d.). Amonio hidroksido faktai. Gauta iš: thinkco.com
- „Pochteca Group“. (2015). Amonio hidroksidas. pochteca.com.mx
- NJ Health (s.f.). Faktinis lapas apie pavojingas medžiagas: amonio hidroksidas. [PDF] Gauta iš: nj.gov
- Chemijos mokytojas. (2018). Amonio hidroksidas. Gauta iš: chemistrylearner.com
- PubChem. (2018). Amonio hidroksidas. Gauta iš: pubchem.ncbi.nlm.nih.gov


