Kalcio fosfatas (Ca3 (PO4) 2) struktūra, savybės, susidarymas ir panaudojimas
The kalcio fosfatas yra neorganinė ir tretinė druska, kurios cheminė formulė yra Ca3(PO4)2. Formulė teigia, kad šios druskos sudėtis yra atitinkamai 3: 2 kalcio ir fosfato. Tai galima matyti tiesiogiai apatiniame vaizde, kuriame rodoma Ca cation2+ ir anijono PO43-. Kas tris Ca2+ Yra du PO43- bendrauti su jais.
Kita vertus, kalcio fosfatas reiškia druskų seriją, kuri skiriasi priklausomai nuo Ca / P santykio, taip pat hidratacijos laipsnio ir pH. Iš tiesų yra daug kalcio fosfatų tipų, kurie egzistuoja ir gali būti sintezuojami. Tačiau, pažodžiui pagal nomenklatūrą, kalcio fosfatas reiškia tik pirmiau minėtą trikalį.

Visi kalcio fosfatai, įskaitant Ca3(PO4)2, Jie yra baltos spalvos, su tamsiomis pilkomis spalvomis. Jie gali būti granuliuoti, smulkūs, kristaliniai ir dalelių dydžiai yra maždaug mikrometrai; ir netgi buvo paruoštos šių fosfatų nanodalelės, su kuriomis suprojektuotos biologiškai suderinamos kaulų medžiagos.
Šis biologinis suderinamumas kyla dėl to, kad šios druskos randamos dantyse ir, trumpai tariant, žinduolių kaulų audiniuose. Pavyzdžiui, hidroksilapatitas yra kristalinis kalcio fosfatas, kuris savo ruožtu sąveikauja su tos pačios druskos amorfine faze.
Tai reiškia, kad yra amorfinių ir kristalinių kalcio fosfatų. Dėl šios priežasties įvairovė ir įvairios galimybės nenuostabu, kai sintezuojamos medžiagos, pagrįstos kalcio fosfatais; medžiagos, kurių savininkai mokslininkai vis labiau domina kiekvieną dieną visame pasaulyje, sutelkdami dėmesį į kaulų atkūrimą.
Indeksas
- 1 Kalcio fosfato struktūra
- 1.1 Amorfinis kalcio fosfatas
- 1.2 Likusi šeimos dalis
- 2 Fizinės ir cheminės savybės
- 2.1 Vardai
- 2.2 Molekulinė masė
- 2.3 Fizinis aprašymas
- 2.4 Skonis
- 2.5 Lydymosi temperatūra
- 2.6 Tirpumas
- 2.7 Tankis
- 2.8 Lūžio rodiklis
- 2.9 Standartinė mokymo entalpija
- 2.10 Laikymo temperatūra
- 2,11 pH
- 3 Mokymas
- 3.1 Kalcio nitratas ir amonio vandenilio fosfatas
- 3.2 Kalcio hidroksidas ir fosforo rūgštis
- 4 Naudojimas
- 4.1 Kaulų audinyje
- 4.2 Biokaminiai cementai
- 4.3 Gydytojai
- 4.4 Kita
- 5 Nuorodos
Kalcio fosfato struktūra
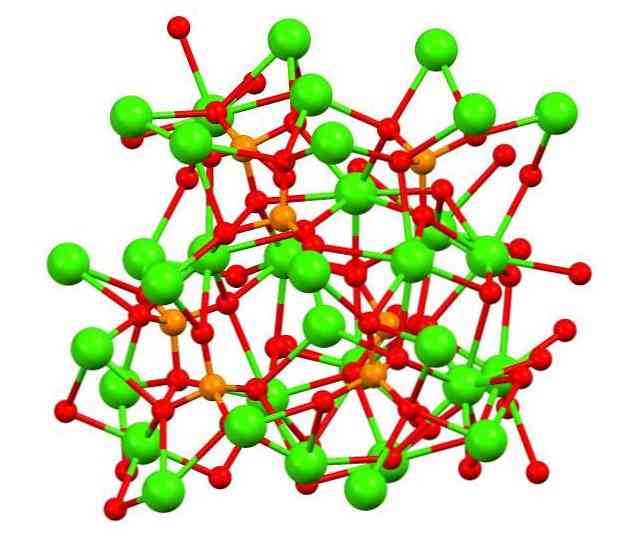
Viršutiniame paveikslėlyje parodyta tribazinio kalio fosfato struktūra keistame baltymingame minerale, kuriame gali būti magnio ir geležies kaip priemaišų..
Nors iš pirmo žvilgsnio tai gali atrodyti sudėtinga, būtina paaiškinti, kad modelis numato kovalentinę sąveiką tarp fosfatų deguonies atomų ir metalo kalcio centrų..
Atstovavimas yra galiojantis, tačiau sąveika yra elektrostatinė; ty katijonai Ca2+ traukia PO anijonai43- (Ca2+- O-PO33-). Turint tai omenyje, suprantama, kodėl vaizde kalcis (žaliosios sferos) yra apsuptas neigiamai įkrautų deguonies atomų (raudonos sferos).
Kai yra tiek daug jonų, jis nepalieka simetriško išdėstymo ar modelio. Ca3(PO4)2 Priima esant žemai temperatūrai (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, už akronimą anglų kalba).
Kita vertus, esant aukštai temperatūrai, ji transformuojama į polimorfą α-Ca3(PO4)2 (α-TCP), kurio vieneto ląstelė atitinka monoklininę kristalinę sistemą. Dar aukštesnėse temperatūrose taip pat gali susidaryti polimorfinis α'-Ca3(PO4)2, kuri yra šešiakampės kristalinės struktūros.
Amorfinis kalcio fosfatas
Buvo paminėtos kalcio fosfato kristalinės struktūros, kurių tikimasi iš druskos. Tačiau jis gali rodyti netvarkingas ir asimetrines struktūras, labiau susietas su "kalcio fosfato stiklo" tipu, o ne kristalais, kaip apibrėžta jo prasme..
Kai taip atsitinka, kalcio fosfatas turi amorfinę struktūrą (AKR, amorfinis kalcio fosfatas). Keletas autorių nurodo, kad tokio tipo struktūra yra atsakinga už Ca biologines savybes3(PO4)2 kaulų audiniuose, jų taisymas ir biomimetizacija yra įmanoma.
Išsiaiškinus jos struktūrą branduolinio magnetinio rezonanso (NMR), nustatyta, kad yra OH jonų- ir HPO42- AKR šalyse. Šie jonai susidaro hidrolizuojant vieną iš fosfatų:
PO43- + H2O <=> HPO42- + OH-
Todėl faktinė AKR struktūra tampa sudėtingesnė, o jo jonų sudėtį sudaro formulė: Ca9(PO4)6-x(HPO4)x(OH)x. „X“ reiškia hidratacijos laipsnį, nes jei x = 1, formulė būtų tokia: Ca9(PO4)5(HPO4) (OH).
Skirtingos struktūros, kurias PCA gali turėti, priklauso nuo Ca / P molinių santykių; ty santykinis kalcio ir fosfato kiekis, kuris keičia visą jų gaunamą kompoziciją.
Likusi šeimos dalis
Kalcio fosfatai iš tikrųjų yra neorganinių junginių šeima, kuri savo ruožtu gali sąveikauti su organine matrica.
Kiti fosfatai yra gaunami „paprasčiausiai“ keičiant kalcio lydinčius anijonus (PO43-, HPO42-, H2PO4-, OH-), taip pat kietųjų medžiagų priemaišų tipą. Taigi, iki vienuolikos ar daugiau kalcio fosfatų, kurių kiekviena turi savo struktūrą ir savybes, gali kilti natūraliai arba dirbtinai..
Toliau pateikiami kai kurie fosfatai ir jų atitinkamos struktūros bei cheminės formulės:
-Vandenilio kalcio fosfato dihidratas, CaHPO4∙ 2H2O: monoklinika.
-Kalcio dihidrofosfato monohidratas, Ca (H)2PO4)2∙ H2O: triklinika.
-Bevandenis fosfatas, Ca (H)2PO4)2: triklinika.
-Ocalcium vandenilio fosfatas (OCP), Ca8H2(PO4)6: triklinika Jis yra hidroksilapatito sintezės pirmtakas.
-Hidroksapatitas, Ca5(PO4)3OH: šešiakampė.
Fizinės ir cheminės savybės
Vardai
-Kalcio fosfatas
-Trikalcio fosfatas
-Trikalcio difosfatas
Molekulinė masė
310,74 g / mol.
Fizinis aprašymas
Tai bekvapė balta kieta medžiaga.
Skonis
Skanus.
Lydymosi temperatūra
1670 K (1391 ° C).
Tirpumas
-Praktiškai netirpsta vandenyje.
-Netirpsta etanolyje.
-Tirpsta praskiestoje druskos rūgštyje ir azoto rūgštyje.
Tankis
3,14 g / cm3.
Lūžio rodiklis
1,629
Standartinė mokymo entalpija
4126 kcal / mol.
Laikymo temperatūra
2-8 ° C.
pH
6-8 kalcio fosfato vandeninėje suspensijoje.
Mokymas
Kalcio nitratas ir vandenilio amonio fosfatas
Kalcio fosfato gamybai arba formavimui yra daug metodų. Vienas iš jų susideda iš dviejų druskų, Ca (NO), mišinio.3)2∙ 4H2O ir (NH4)2HPO4, anksčiau ištirpinti absoliučiame alkoholyje ir vandenyje. Vienoje druskoje yra kalcio ir kitas fosfatas.
Iš šio mišinio išsiskiria AKR, kuri tada kaitinama orkaitėje 800 ° C temperatūroje ir 2 valandas. Šios procedūros metu gaunamas β-Ca3(PO4)2. Kruopščiai kontroliuojant temperatūrą, maišymą ir kontaktinius laikus gali susidaryti nanokristalinis susidarymas.
Sudaryti polimorfo-Ca3(PO4)2 būtina šildyti fosfatą virš 1000 ° C. Šis kaitinimas atliekamas dalyvaujant kitiems metaliniams jonams, kurie stabilizuoja šį polimorfą, kad jį būtų galima naudoti kambario temperatūroje; tai yra, jis lieka stabilioje meta būsenoje.
Kalcio hidroksidas ir fosforo rūgštis
Kalcio fosfatas taip pat gali būti susidaręs maišant kalcio hidroksido ir fosforo rūgšties tirpalus su rūgšties ir bazės neutralizavimu. Po pusę tos dienos, kai buvo brandinami tirpalai, ir tinkamai filtruojant, plaunant, džiovinant ir sijojant, gaunamas granuliuotas amorfinio fosfato milteliai, AKR.
Ši AKR reakcija sukuria aukštą temperatūrą, transformuojančią pagal šias chemines lygtis:
2Ca9(HPO4) (PO4)5(OH) => 2Ca9(P2O7)0,5(PO4)5(OH) + H2O (esant T = 446,60 ° C)
2Ca9(P2O7)0,5(PO4)5(OH) => 3Ca3(PO4)2 + 0,5H2O (esant T = 748,56 ° C)
Tokiu būdu gaunamas β-Ca3(PO4)2, labiausiai paplitęs ir stabilus polimorfas.
Naudojimas
Kaulų audinyje
Ca3(PO4)2 Tai pagrindinė neorganinė kaulų pelenų sudedamoji dalis. Tai yra kaulų pakeitimo transplantatų sudedamoji dalis, kurią paaiškina jo cheminis panašumas su kauluose esančiais mineralais.
Kalcio fosfato biomedžiagos naudojamos kaulų defektams ir titano metalo protezų padengimui. Kalcio fosfatas kaupiasi ant jų, išskiriant juos iš aplinkos ir sulėtinant titano korozijos procesą.
Kalcio fosfatai, įskaitant Ca3(PO4)2, Jie naudojami keraminių medžiagų gamybai. Šios medžiagos yra biologiškai suderinamos ir šiuo metu naudojamos atkurti alveolinį kaulų praradimą, atsirandantį dėl periodonto ligos, endodontinių infekcijų ir kitų sąlygų..
Tačiau jie turėtų būti naudojami tik spartesniam kaulų remontui paspartinti tose vietose, kuriose nėra lėtinės bakterinės infekcijos.
Kalcio fosfatas gali būti naudojamas kaulų defektų taisymui, kai negalima naudoti autogeninio kaulų transplantato. Jį galima naudoti atskirai arba kartu su biologiškai skaidomu ir rezorbuojančiu polimeru, pvz., Poliglikolio rūgštimi..
Biokeraminiai cementai
Kalcio fosfato cementas (CPC) yra dar vienas biokeramikas, naudojamas kaulų audinių remontui. Jis gaminamas sumaišant įvairių tipų kalcio fosfatų miltelius su vandeniu, formuojant pastą. Pasta gali būti švirkščiama arba priderinta prie kaulo defekto ar ertmės.
Cementai formuojami, palaipsniui resorbuojami ir pakeičiami naujai suformuotu kaulu.
Gydytojai
-Ca3(PO4)2 Tai bazinė druska, todėl ji naudojama kaip antacidinis preparatas neutralizuojant skrandžio rūgšties perteklių ir padidinant pH. Dantų pasta suteikia kalcio ir fosfato šaltinį, kuris palengvina dantų ir kaulų hemostazės remineralizacijos procesą..
-Jis taip pat naudojamas kaip maisto papildas, nors pigiausias būdas pakeisti kalcį yra jo karbonato ir citrato naudojimas..
-Kalcio fosfatas gali būti naudojamas gydant tetaną, latentinę hipokalcemiją ir palaikomąją terapiją. Be to, jis yra naudingas kalcio papildymui nėštumo ir žindymo laikotarpiu.
-Jis naudojamas radioaktyviųjų izotopų radijo (Ra-226) ir stroncio (Sr-90) užteršimui gydyti. Kalcio fosfatas blokuoja radioaktyviųjų izotopų absorbciją virškinimo trakte, taip sumažindamas jų sukeltą žalą.
Kiti
-Kalcio fosfatas naudojamas kaip paukščių pašaras. Be to, jis naudojamas dantų pastos kontroliuojant akmenį.
-Jis naudojamas kaip antikorozinis agentas, pavyzdžiui, neleidžiant suspausti stalo druska.
-Jis veikia kaip miltų balinimo priemonė. Nors kiaulienos kiaulytė apsaugo nuo nepageidaujamos spalvos ir pagerina kepimo būklę.
Nuorodos
- Tung M.S. (1998) Kalcio fosfatai: struktūra, sudėtis, tirpumas ir stabilumas. In: Amjad Z. (red.) Kalcio fosfatai biologinėse ir pramoninėse sistemose. Springer, Boston, MA.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu ir Honglian Dai. (2018). „Nano-β-trikalcio fosfato sintezė, apibūdinimas ir hepatoceliulinės karcinomos ląstelių slopinimas“, Journal of Nanomaterials, t. 2018 m., ID 7083416, 7 puslapiai, 2018 m.
- Kovos, Kristus ir Rey, krikščionys. (2010). Amorfiniai kalcio fosfatai: sintezė, savybės ir panaudojimas biomaterijose. Acta Biomaterialia, t. 6 (Nr. 9). pp. 3362-3378. ISSN 1742-7061
- Vikipedija. (2019). Trikalcio fosfatas. Gauta iš: en.wikipedia.org
- Abida ir kt. (2017). Trikalcio fosfato milteliai: paruošimo, apibūdinimo ir tankinimo gebėjimai. „Mediterranean Journal of Chemistry 2017“, 6 (3), 71-76.
- PubChem. (2019). Kalcio fosfatas. Gauta iš: pubchem.ncbi.nlm.nih.gov
- Elsevier (2019). Kalcio fosfatas. „Science Direct“. Gauta iš: sciencedirect.com


