Aliuminio chlorido (AlCl3) cheminė struktūra, savybės, panaudojimas
The aliuminio chloridas arba aliuminio trichloridas (AlCl3) yra dvejetainė druska, sudaryta iš aliuminio ir chloro. Kartais jis atrodo kaip geltonasis milteliai, nes jis turi priemaišų dėl geležies (III) chlorido.
Jis gaunamas derinant jo elementus. Aliuminis, kurio paskutiniame energijos lygmenyje yra trys elektronai (IIIA šeima), yra linkęs jas duoti dėl savo metalo. Chloras su septyniais elektronais paskutiniame energijos lygmenyje (VIIA šeima) yra linkęs įgyti juos užbaigti oktetą.
Manoma, kad aliuminio ir chloro aliuminio trichloride jungtis yra kovalentinė, nors tai yra metalo ir ne metalo jungtis..
Yra dviejų rūšių aliuminio chloridas:
- Bevandenis aliuminio chloridas. AlCl3.
- Aliuminio chlorido heksahidratas. AlCl3. 6H2O. Šis junginys randamas kietoje arba tirpalo formoje.
Indeksas
- 1 Cheminė struktūra
- 2 Ypatybės
- 2.1 Fizinis
- 2.2 Cheminės medžiagos
- 3 Naudojimas
- 4 Rizika: galimas poveikis
- 5 rekomendacijos
- 6 Nuorodos
Cheminė struktūra
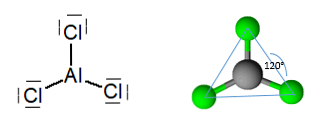
Bevandenis aliuminio trichloridas yra molekulė, turinti plokštuminę trigoninę geometriją, kurios kampas yra 120 °, atitinkantis atominį hibridizacijos \ t2.
Tačiau molekulė yra organizuota dimeriai, kurioje chloro atomas dovanoja elektronų porą, kad suformuotų ryšius. Tai vadinama koordinuotomis kovalentinėmis obligacijomis.
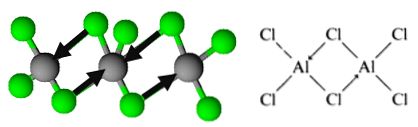
Taip išvada aliuminio trichlorido dimerių organizavimą.
Ši organizacija leidžia junginiui formuoti dimerinius sluoksnius. Kai vanduo yra pilamas ant kieto aliuminio trichlorido, jie nesiskiria, kaip tikėtasi, iš joninių junginių, bet intensyviai hidrolizuojasi.
Priešingai, praskiestame vandeniniame tirpale yra koordinuoti jonai [Al (H2O)6]+3 ir chlorido. Šios struktūros yra labai panašios į diborano struktūras.
Tokiu būdu turite formulę Al2Cl6
Jei matuojamas šio junginio junginių elektronų elektroninio skirtumo skirtumas, galima pastebėti:
Aliuminio A atveju elektronegatyvumo vertė yra 1,61 C, o chloro vertė - 3,16 C. Elektronegatiškumo skirtumas yra 1,55 C.
Pagal privalomosios teorijos taisykles, kad junginys būtų joninis, jis turi turėti skirtumą tarp atomų, sudarančių ryšį, kurio vertė didesnė arba lygi 1,7 C.
Esant Al-Cl ryšiui, elektronegatyvumo skirtumas yra 1,55 C, o tai suteikia aliuminio trichlorido kovalentinio susiejimo. Šią nedidelę vertę galima priskirti molekulės pateiktoms koordinuotoms kovalentinėms jungtims.
Savybės
Fizinis
Išvaizda: balta kieta medžiaga, kartais geltona dėl geležies chlorido sukeltų priemaišų
Tankis: 2,48 g / ml
Molinė masė133,34 g / mol
Sublimacija: sublimuojama 178 ° C temperatūroje, todėl jo lydymosi ir virimo taškai yra labai mažai.
Vairavimas: prastai atlieka elektros energiją.
Tirpumas: jis netirpsta vandenyje, nes jis yra Lewis rūgštis. Jis tirpsta organiniuose tirpikliuose, tokiuose kaip benzenas, anglies tetrachloridas ir chloroformas.
Chemikalai
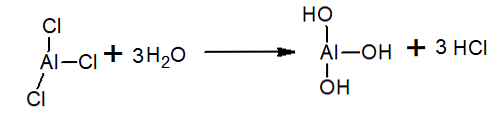
Vandenyje aliuminio trichloridas hidrolizuojamas, sudarant HCl ir hidronio joną bei aliuminio hidroksidą:
Jis naudojamas Friedel-Crafts reakcijose kaip katalizatorius (medžiaga, kurią galima atkurti reakcijos pabaigoje, nes tik joje pagreitinama, sulėtinama arba pradėta reakcija)..
Tai yra ėsdinanti medžiaga.
Skilimo metu, kai jis smarkiai reaguoja su vandeniu, susidaro aliuminio oksidas ir pavojingos dujos, pvz., Vandenilio chloridas.
Naudojimas
- Antiperspirantas.
- Friedel-Crafts acilinimo ir alkilinimo katalizatorius.
Rizika: galimas poveikis
- Tai yra ėsdinanti medžiaga, sukelia odos nudegimus ir sunkius akių pažeidimus.
- Smarkiai reaguoja su vandeniu.
- Tai pavojinga aplinkai.
- Labai toksiška vandens organizmams.
Rekomendacijos
Venkite produkto patekimo be būtinų saugos priemonių. Turi būti naudojami apsauginiai akiniai, pirštinės, tinkami drabužiai, padengti batai.
Įkvėpus. Dulkių įkvėpimas gali dirginti kvėpavimo takus dėl medžiagos korozijos. Simptomai yra gerklės skausmas, kosulys ir dusulys. Plaučių edemos simptomai gali būti pavėluoti ir sunkūs atvejai gali būti mirtini. Nukelkite nukentėjusįjį į erdvią vietą be teršalų. jei reikia, suteikti dirbtinį kvėpavimą. Jei sunku kvėpuoti, duokite deguonį. Kreipkitės į gydytoją.
Patekus ant odos. AlCl3 Jis yra ėsdinantis. Jis gali sukelti sudirginimą ar nudegimus, pasireiškiančius paraudimu ir skausmu. Nedelsiant nuplauti dideliu kiekiu vandens mažiausiai 20 minučių. Negalima neutralizuoti ar pridėti kitų medžiagų nei vanduo. Pašalinkite užterštus drabužius ir nuplaukite prieš pakartotinį naudojimą. nedelsiant kreipkitės į gydytoją sužalojimo atveju.
Patekus į akis. AlCl3 Jis yra ėsdinantis. Jis sukelia stiprų skausmą, neryškų matymą ir audinių pažeidimą. Nedelsiant skalauti akis mažiausiai 20 minučių vandeniu ir laikyti akis vokus, kad būtų užtikrinta, jog visos akies akys ir audiniai išvalomi. Norint pasiekti maksimalų efektyvumą, akių skalavimas per kelias sekundes yra labai svarbus. Jei turite kontaktinius lęšius, nuimkite juos po pirmųjų 5 minučių ir po to tęskite akis. Pasitarkite su gydytoju. Jis gali sukelti rimtą žalą ragenos, junginės ar kitoms akies dalims.
Prarijus. AlCl3 Jis yra ėsdinantis. Deginimas gali sukelti burnos ir stemplės skausmą bei gleivinių nudegimus. Jis gali sukelti skrandžio ir žarnyno diskomfortą su pilvo skausmu, pykinimu, vėmimu ir viduriavimu. NEGALIMA VOMITŲ. Išskalaukite burną ir gerkite vandenį. Niekada neduokite jokių žodžių sąmonės neturinčiam asmeniui. Kreipkitės į gydytoją. Jei vėmimas įvyksta savaime, nukentėjusįjį nukreipkite į savo pusę, kad sumažėtų aspiracijos rizika.
Žmonės, turintys esamų odos sutrikimų ar akių sutrikimų ar sutrikusi kvėpavimo funkcija, gali būti jautresni medžiagos poveikiui
AlCl junginio pakavimas ir laikymas3 turi būti atliekama vėdinamoje, švarioje ir sausoje vietoje.
Nuorodos
- Cheminė knyga, (2017), Aliuminio chloridas. Atgautas iš chemijos knygos.com
- kosmosas internete, cosmos.com.mx
- Sharpe, A.G., (1993), Organic Chemistry, Ispanija, Redakcijos Reverté, S.A..
- F., (2017), AlCl aliuminio chloridas3, Ženklai. Paimta išblog.elinsignia.com.
- TriHealth, (2018), aliuminio trichloridas, paskutinis atnaujinimas, 2018 m. Kovo 4 d., Gauta iš trihealth.adam.com.
- RxWiki, (s.f), aliuminio chloridas, Gauta iš, rxwiki.com.


