Butino struktūra, savybės ir panaudojimas
The butino yra cheminis junginys, priklausantis alkinų grupei, kuriai būdinga mažiausiai trijų jungčių tarp dviejų anglies atomų struktūra..
Kalbant apie alkynų pavadinimo taisyklių nustatymą, IUPAC (Tarptautinės grynosios ir taikomosios chemijos sąjungos akronimas anglų kalba) nustatė, kad jie naudojami taip pat, kaip ir alkenams..

Esminis abiejų medžiagų tipų nomenklatūros skirtumas yra tas, kad sufiksas -on pakeistas į - kai kalbama apie junginius, kurių struktūra yra triguba..
Kita vertus, butinas susideda tik iš anglies ir vandenilio ir yra dviejų formų: 1-butinas, kuris yra dujų fazėje esant standartinėms slėgio ir temperatūros sąlygoms (1 atm, 25 ° C); ir 2-butino, kuris yra cheminės sintezės būdu gauta skystosios fazės rūšis.
Indeksas
- 1 Cheminė struktūra
- 1.1 1-butino
- 1.2 2-butinas
- 2 Ypatybės
- 3 Naudojimas
- 4 Nuorodos
Cheminė struktūra
Molekulėje, vadinamoje butinu, pateikiamas padėties struktūrinio izomerizavimo reiškinys, kuris susideda iš tų pačių funkcinių grupių buvimo abiejuose junginiuose, tačiau kiekvienas iš jų yra kitoje grandinės vietoje..
Šiuo atveju abi butino formos turi identišką molekulinę formulę; tačiau 1-butyne trikampis ryšys yra anglies numeris vienas, o 2-butyne - antrasis. Tai konvertuoja juos į vietos izomerus.
Dėl trijų jungčių buvimo viename iš 1-butininės struktūros gnybtų jis laikomas galiniu alkinu, o trikampio jungties tarpinė padėtis 2-butininėje struktūroje suteikia jai vidinės alkinės klasifikaciją..
Taigi, ryšys gali būti tik tarp pirmojo ir antrojo anglies (1-butino) arba tarp antrojo ir trečiojo anglies (2-butino). Taip yra dėl to, kad taikoma nomenklatūra, kurioje visuomet bus suteikta kuo mažesnė numeracija.
1-butino
Junginys, vadinamas 1-butinu, taip pat žinomas kaip etilacetilenas, dėl jo struktūros ir keturių anglies atomų išdėstymo ir surišimo. Tačiau kalbant apie butino daroma nuoroda tik į šias chemines rūšis.
Šioje molekulėje trigubas ryšys randamas galinėje anglies, kuri leidžia gauti vandenilio atomų, kurie suteikia jam didelį reaktyvumą.
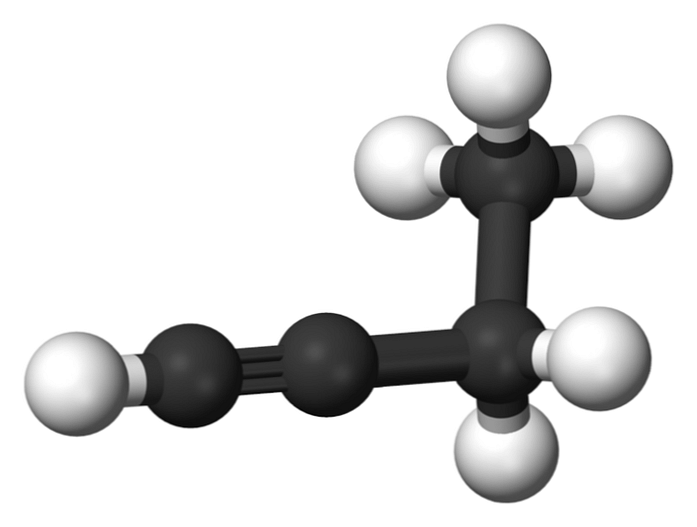
Ši standi ir stipresnė jungtis, nei viena arba dviguba jungtis tarp anglies atomų, užtikrina stabilią 1-butininės linijinės geometrijos konfigūraciją.
Kita vertus, ši dujinė medžiaga yra gana degi, todėl esant karščiui, ji gali lengvai sukelti gaisrą ar sprogimą ir turi didelį reaktyvumą esant orui ar vandeniui..
2-butinas
Kadangi vidaus alkynai turi didesnį stabilumą nei galiniai alkinai, jie leidžia transformuoti 1-butiną į 2-butiną.
Šis izomerizavimas gali įvykti kaitinant 1-butiną, dalyvaujant bazei (pvz., NaOH, KOH, NaOCH3 ...) arba perorganizuojant 1-butiną kalio hidroksido (KOH) tirpale etanolyje (C2H6O).
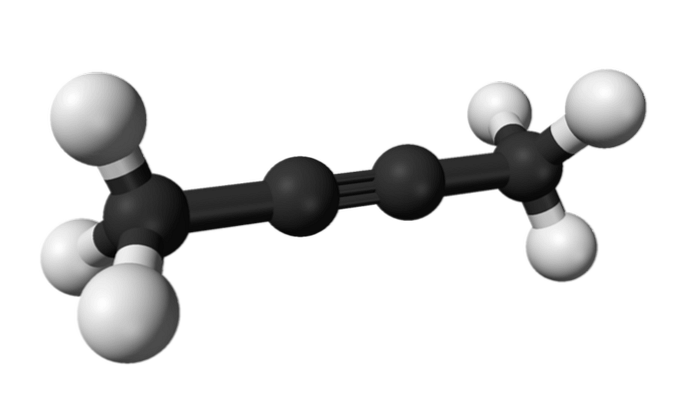
Taip pat cheminė medžiaga, vadinama 2-butinu, taip pat vadinama dimetilacetilenu (arba krotonilenu), kuris yra skystas ir lakus, dirbtinai kilęs..
2-butyne, trigubas ryšys yra molekulės viduryje, suteikiant jam didesnį stabilumą nei jo izomeras.
Be to, šis bespalvis junginys turi mažesnį tankį nei vanduo, nors jis yra netirpus jo ir turi didelį degumą.
Savybės
-Struktūrinė butino formulė (nepriklausomai nuo to, kuriam izomerui nurodoma) yra C4H6, kuri turi linijinę struktūrą.
-Viena iš cheminių reakcijų, kurias patyrė butino molekulė, yra izomerizacija, kurioje molekulėje vyksta trimatės jungties pertvarkymas ir migracija..
-1-Butyne yra dujų fazėje, turi labai didelį degumą ir didesnį tankį nei oras.
-Ši medžiaga taip pat yra gana reaktyvi ir, esant šilumai, gali sukelti smurtinius sprogimus.
-Be to, kai ši bespalvė dujos patiria nepakankamą degimo reakciją, tai gali sukelti anglies monoksidą (CO).
-Kai abu izomerai yra veikiami aukštoje temperatūroje, jie gali patirti sprogstamųjų polimerizacijos reakcijų.
-2-butinas yra skystoje fazėje, nors jis taip pat laikomas gana degiu esant standartinėms slėgio ir temperatūros sąlygoms.
-Šios medžiagos gali patirti smurtinių reakcijų, kai yra stiprių oksiduojančių medžiagų.
-Taip pat eksoterminės reakcijos, dėl kurių išsiskiria dujinis vandenilis, atsiranda esant redukuojančioms rūšims..
-Esant sąlyčiui su tam tikrais katalizatoriais (pvz., Kai kuriomis rūgštinėmis medžiagomis) arba pradinių rūšių, gali atsirasti egzoterminės polimerizacijos reakcijos..
Naudojimas
Kadangi jie turi tam tikrų skirtingų savybių, abu izomerai gali turėti skirtingus naudojimo būdus ir programas, kaip parodyta toliau:
Visų pirma, labai dažnai vienas iš 1-butino panaudojimas yra jo naudojimas kaip tarpinis cheminių medžiagų, turinčių sintetinių medžiagų, gamybos proceso etapas..
Kita vertus, ši cheminė medžiaga naudojama gumos ir jų junginių gamybos pramonėje; pavyzdžiui, kai norite gauti benzolą.
Panašiai jis naudojamas įvairių plastikinių gaminių gamybos procese, taip pat daugelio polietileno medžiagų, kurios laikomos dideliu tankumu, gamyboje..
Be to, kai kurių metalo lydinių, įskaitant plieną (geležies lydinį ir anglies), pjovimo ir suvirinimo procesuose dažnai naudojamas 1-butinas..
Kitaip tariant, 2-butinino izomeras naudojamas kartu su kitu alkinu, vadinamu propinu, kai kurių medžiagų, vadinamų alkilintomis hidrochinonais, sintezėje, kai atliekamas visiškas α-tokoferolio (vitamino E) sintezės procesas.
Nuorodos
- Vikipedija. (s.f.). Butyne Gauta iš en.wikipedia.org
- Yoder, C. H., Leber P. A. ir Thomsen, M. W. (2010). Tiltas į organinę chemiją: sąvokos ir nomenklatūra. Gauta iš books.google.co.ve
- Study.com. (s.f.). Butynas: struktūrinė formulė ir izomerai. Gauta iš tyrimo.
- PubChem. (s.f.). 1-Butyne. Gauta iš pubchem.ncbi.nlm.nih.gov
- PubChem. (s.f.). 2-Butyne. Gauta iš pubchem.ncbi.nlm.nih.gov


