Natrio acetato formulė, paruošimas, savybės, rizika ir panaudojimas
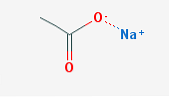
The natrio acetatas, taip pat žinomas kaip natrio etanoatas (sutrumpintas kaip NaOAc), yra acto rūgšties natrio druska. Jo cheminė formulė yra CH3COONa ir turi joninį ryšį tarp natrio jono ir acetato jonų.
Šis cheminis junginys natūraliai yra augalų ir gyvūnų audiniuose. Jis gali būti bet kokia forma, bevandenis arba trihidratuotas. Abu jonai, Na + ir CH3COO- yra organizmuose ir atlieka gyvybines funkcijas: natrio joną kaip viso kūno vandens reguliatorių ir acetato joną kaip vandenilio akceptorių (natrio acetato formulė, 2005-2017).
Indeksas
- 1 Paruošimas
- 2 Fizinės ir cheminės savybės
- 3 Reaktingumas ir pavojai
- 4 Naudojimas ir sandėliavimas
- 5 Naudojimas ir taikymas
- 6 Nuorodos
Paruošimas
Natrio acetatas yra junginys, kuris gali būti paruoštas paprastu ir prieinamu būdu visiems. Paprastai jo paruošimas yra žinomas kaip „karšto ledo eksperimentas“, nes kristalizacija primena kietojo kūno vandenį (mokslininkas, 2016)..
Norint paruošti natrio acetatą, reikia tik acto (acto rūgšties) ir natrio karbonato arba natrio bikarbonato. Tiesiog įpilkite bikarbonato prie acto, susidarant putojančiai reakcijai, nes ji išskiria anglies dioksidą pagal reakcijas.
CH3COOH + NaHCO3 → CH3COONa + H2CO3
H2CO3 → CO2 + H2O
Karbonatas arba natrio bikarbonatas gali būti pakeistas natrio hidroksidu (šarmu), kur pagal reakciją gaminamas natrio acetatas ir vanduo:
CH3COOH + NaOH → CH3COONa + H2O
Ši reakcija nesukelia svaiginimo, tačiau turi trūkumų, kad natrio hidroksido yra sunkiau apdoroti nei bikarbonatas.
Kad būtų pasiektas kristalizacijos efektas (arba karšto ledo poveikis), tirpalas turi būti perpildytas šildant jį, kad būtų ištirpintas bikarbonatas. Tada uždarytas indas atšaldomas ir po to perkristalinamas. Vėliau kristalai filtruojami ir susmulkinami saugoti (degroof, S.F.)..
Fizinės ir cheminės savybės
Natrio acetatas yra baltas higroskopinis stiklas su acto kvapu.

Jei junginys yra bevandenis, jo molekulinė masė yra 82,03 g / mol ir tankis yra 1,5 g / ml. Jo lydymosi temperatūra yra 324 laipsniai, o jo virimo temperatūra yra 881,4 laipsnių.
Trihidratuotos formos molekulinė masė yra 136,03 g / mol ir tankis 1,45 g / ml. Lydymosi ir virimo taškai drastiškai sumažėja iki 58 laipsnių Celsijaus ir 122 laipsnių Celsijaus.
Natrio acetatas labai gerai tirpsta vandenyje. Trihidrato formos tirpumas yra 46,5 g natrio acetato 100 ml vandens 20 laipsnių Celsijaus, o bevandenėje formoje gali ištirpinti 123 gramus 100 ml vandens (Nacionalinis biotechnologijų informacijos centras, 2017 m. ).
Abi formos tirpsta acetone, metanolyje, hidrazine ir trihidrato forma tirpsta etanolyje. Natrio acetatas turi monoklininę kristalinę struktūrą (Royal Society of Chemistry, 2015).
Natrio acetatas yra acto rūgšties konjuguota bazė, todėl galite naudoti acto rūgšties / natrio acetato tirpalą, kad paruoštų buferinius tirpalus, kad būtų galima kontroliuoti pH..
Natrio acetato tirpalas vandenyje yra silpnai šarminis. Kai šiluma yra didesnė nei 324 laipsniai Celsijaus, ši druska suskaidosi, susidarant acto rūgšties garams.
Reaktingumas ir pavojai
Natrio acetatas klasifikuojamas kaip stabilus junginys ir nesuderinamas su oksiduojančiais agentais. Įkaitinus gali susidaryti acto rūgšties garai ir CO2. Junginys gali būti degus esant aukštai temperatūrai, atleidžiantis CO ir CO2.
Natrio acetato saugumas buvo išsamiai ištirtas žiurkių ir pelių gyvūnų modeliuose. Vartojant per burną, mirtina dozė, kuri žudo pusę žiurkių populiacijos, yra 3530 mg natrio acetato 1 kg žiurkės kūno svorio..
Įkvėpus vietoj nurijus, pusė žiurkių populiacijos nužudymui reikalinga dozė yra daug didesnė, daugiau nei 30 g / m3 per valandą.
Pelėms po 3200 mg / kg kūno svorio po oda ar po oda švirkščiama pusė pelių, panašiai kaip nurijus natrio acetato žiurkėms..
Tačiau pelėms, vartojamoms per burną, jos gali atlaikyti daug daugiau negu žiurkės; tai yra mirtina dozė pusėms 6891 mg / kg kūno svorio pelių.
Žmonėms įkvėpus natrio acetatas gali atsirasti kosulys ir gerklės skausmas, o tiesioginis sąlytis su oda arba akimis gali sukelti paraudimą ir dirginimą. Tačiau apskritai toksinis poveikis žmonėms yra minimalus (WASSERMAN, 2015).
Jis gali sukelti virškinimo trakto dirginimą pilvo skausmu, pykinimu, vėmimu ir paveikti šlapimo sistemą. Junginio įkvėpimas gali sukelti kvėpavimo takų dirginimą. Simptomai gali būti kosulys, gerklės skausmas, dusulys ir krūtinės skausmas.
Patekus į akis, kontaktinius lęšius reikia patikrinti ir pašalinti. Akys turi būti nedelsiant plaunamos dideliu kiekiu vandens mažiausiai 15 minučių. Galite naudoti šaltą vandenį. Jei dirginimas pasireiškia, reikia kreiptis į gydytoją.
Patekus ant odos, reikia nuplauti muilu ir vandeniu. Galite naudoti šaltą vandenį. Dirginanti oda yra padengta minkštinančia medžiaga. Jei dirginimas atsiranda, kaip ir patekus į akis, reikia kreiptis į gydytoją.
Jei jis yra įkvėptas, nukentėjusysis turi būti perkeltas į vėsią vietą. Jei nėra kvėpavimo, reikia naudoti dirbtinį kvėpavimą. Jei kvėpavimas yra sunkus, reikia duoti deguonį. Dar kartą reikia nedelsiant kreiptis į gydytoją.
Prarijus, vėmimas neturėtų būti skatinamas, nebent medicinos personalas tai aiškiai nurodė. Niekada nieko neduokite į burną sąmonės neturinčiam asmeniui.
Laisvus drabužius, tokius kaip marškinių apykaklė, kaklaraištis ar diržas, reikia atlaisvinti. Jei pasireiškia simptomai, reikia kreiptis į gydytoją (medžiagos saugos duomenų lapas bevandenis natrio acetatas, 2013 m.).
Naudojimas ir saugojimas
-Junginys turi būti laikomas atokiau nuo šilumos ir uždegimo šaltinių
-Tuščios talpyklos kelia gaisro pavojų, likučius išgaruoja po gaubtu
-Elektriniai įrenginiai turi būti įžeminti, kad būtų išvengta kibirkščių
-Negalima nuryti ar įkvėpti dulkių
-Turi būti dėvimi tinkami apsauginiai drabužiai
-Jei trūksta ventiliacijos, reikia dėvėti tinkamas kvėpavimo priemones
-Prarijus reikia nedelsiant kreiptis į gydytoją ir parodyti pakuotę arba etiketę
-Reagentas turi būti laikomas atokiau nuo nesuderinamų medžiagų, tokių kaip oksidatoriai ir rūgštys.
-Pakuotę laikykite sandariai uždarytą, be to, laikykite indą vėsioje ir gerai vėdinamoje vietoje.
Naudojimas ir taikymas
Natrio acetatas naudojamas labai įvairiose pramonės šakose. Tekstilės pramonėje natrio acetatas neutralizuoja sieros rūgšties atliekų srautus ir taip pat kaip fotorezistą, naudojant anilino dažus. Tai pagerina gatavų audinių kokybę.
Nuotraukoje natrio acetatas yra kūrėjo sprendimo dalis ir veikia kaip fotorezistas. Natrio acetatas naudojamas mažinti vandens sukeltą betonui padarytą žalą, veikiant kaip hermetikas, nors ir aplinkai palankus ir pigesnis už įprastą epoksidinę alternatyvą betonui užsandarinti vandeniu..
Jis taip pat yra chromo rauginimo marinavimo agentas ir padeda išvengti klopopreno vulkanizavimo sintetinės gumos gamyboje. Vienkartinės medvilnės pagalvėlės medvilnės perdirbimo procese natrio acetatas naudojamas statinei elektros energijos kaupimui pašalinti.
Natrio acetatas, įdėtas į maistą, veikia kaip konservantas ir kvapiosios medžiagos. Visų pirma, bulvių traškučiai su natrio acetatu pasižymi skiriamuoju „druskos ir acto“ skoniu.
Natrio acetatas taip pat naudojamas šildymo pagalvėlėse, rankų šildytuvuose ir karštu ledu. Trihidrato natrio acetato kristalai ištirpinami 58,4 ° C temperatūroje, ištirpinant jų kristalizacijos vandenyje.
Kai šildomas už lydymosi temperatūros ir po to leidžiama atvėsti, vandeninis tirpalas tampa perpildytas. Šis tirpalas gali atvėsti iki kambario temperatūros nesukuriant kristalų.
Spaudžiant metalinį diską į kaitinimo padėklą, susidaro brandinimo centras, todėl tirpalas kristalizuojamas atgal į kietą natrio acetato trihidratą. Kristalizacijos ryšių formavimo procesas yra egzoterminis. Paslėpta sintezės šiluma yra maždaug 264-289 kJ / kg.
Skirtingai nuo kai kurių šilumos pakuočių tipų, pvz., Nuo negrįžtamų cheminių reakcijų, natrio acetato šilumos paketas gali būti lengvai panaudojamas panardinant pakuotę į verdantį vandenį keletą minučių, kol kristalai visiškai ištirps ir leidžia kad pakuotė lėtai atvės, kol pasieks kambario temperatūrą.
Natrio acetato ir acto rūgšties tirpalai veikia kaip buferiai, palaikantys santykinai pastovų pH, naudingą savybę tiek biocheminėms tyrimų reakcijoms, tiek naftos pramonei ir kosmetikos pramonei..
Natrio acetatas gali būti naudojamas mažoms nukleino rūgštims nusodinti. Šis nusodinimas gali būti naudojamas mažoms nukleino rūgštims koncentruoti iš atskiestų tirpalų, pvz., Žemesnio veikimo buferio, po frakcijos frakcionavimo..
Kai į flashPAGE smulkintuvą įkraunama mažiau kaip 2 μg nukleorūgšties, rekomenduojama per naktį nusodinti natrio acetatu / etanoliu, pvz., Su linijiniu akrilamidu arba glikogenu, kad maksimaliai išgautų nukleino rūgštį iš veikimo buferio lėtai.
Glikogeno, kaip nešiklio, naudojimas nerekomenduojamas mėginiams, kurie bus naudojami DNR lustų analizei (nedidelių nukleino rūgščių natrio acetato nuosėdos, S.F.)..
Medicinos srityje natrio acetato tirpalai gydo pacientus, kuriems yra didelis kraujo rūgšties kiekis ir (arba) mažas natrio kiekis.
Natrio yra pagrindinis ekstraląstelinio skysčio katijonas. Jis sudaro daugiau kaip 90% visų katijonų, esant normaliai koncentracijai plazmoje - maždaug 140 mEq / l. Natrio jonas atlieka pagrindinį vaidmenį kontroliuojant viso kūno vandens kiekį ir jo pasiskirstymą (natrio acetatas, 2010)..
Acetatas yra vandenilio jonų akceptorius. Jis taip pat tarnauja kaip alternatyvus bikarbonato (HCO3-) šaltinis metaboliniam konversijai kepenyse. Nustatyta, kad ši konversija vyksta lengvai, net ir esant sunkiai kepenų ligai.
Vandeniu praskiestą natrio acetato injekciją į veną leidžiama kaip elektrolitų papildymo priemonę. Kiekviename 20 ml yra 3,28 g natrio acetato, kuriame yra 40 mEq natrio (Na +) ir acetato (HCO).3-). Tirpalo sudėtyje nėra bakteriostato, antimikrobinių medžiagų ar pridėto buferio. Jame gali būti acto rūgšties pH reguliavimui (pH yra 6,5 (6,0–7,0)). Ozololio koncentracija yra 4 mOsmol / ml (apskaičiuota).
Manoma, kad tirpalas yra alternatyva natrio chloridui, kad būtų užtikrintas natrio jonas (Na +), skirtas papildyti didelio tūrio infuzinius skysčius intraveniniam vartojimui (natrio acetatas, 2009)..
Natrio jonus turintys tirpalai turi būti naudojami labai atsargiai, ypač pacientams, sergantiems staziniu širdies nepakankamumu, sunkiu inkstų nepakankamumu ir klinikinėmis sąlygomis, kai yra edema su natrio sulaikymu..
Pacientams, kurių inkstų funkcija sutrikusi, natrio jonų turinčių tirpalų skyrimas gali sukelti natrio sulaikymą. Tirpalai, kurių sudėtyje yra acetato jonų, turi būti naudojami labai atsargiai pacientams, kuriems yra metabolinė ar kvėpavimo alkalozė.
Acetatas turi būti skiriamas labai atsargiai tomis sąlygomis, kai padidėja šio jono kiekis arba sumažėja jo panaudojimas, pvz., Sunkus kepenų nepakankamumas..
Nuorodos
- (S.F.). Kaip gaminti natrio acetatą iš buitinių ingredientų. Recuperado de instructables: instructables.com.
- Medžiagos saugos duomenų lapas Bevandenis natrio acetatas. (2013 m. Gegužės 21 d.). Gauta iš sciencelab: sciencelab.com.
- Nacionalinis biotechnologijų informacijos centras. (2017 m. Kovo 4 d.). „PubChem Compound“ duomenų bazė; CID = 517045. Gauta iš „PubChem“.
- Karališkoji chemijos draugija. (2015). Natrio acetatas. Gauta iš chemspider.com.
- mokslininkas D. N.-c. (2016 m. Rugpjūčio 12 d.). „HOT ICE“ - nuostabus eksperimentas. Gauta iš „youtube.com“.
- Natrio acetatas. (2009 m. Gegužės 19 d.). Gauta iš rxlist.
- Natrio acetatas. (2010 m. Balandžio mėn.). Susigrąžinta iš drug.com.
- Natrio acetatas. (2005-2017). Atkurta iš softschools.com.
- Mažų nukleino rūgščių natrio acetato nusodinimas. (S.F.). Išgautas iš termofikatoriaus.
- WASSERMAN, R. (2015 m. Rugpjūčio 16 d.). Kas yra natrio acetato druska? Gauta iš livestrong: livestrong.com.


