Atominis tūris Kaip jis skiriasi periodinėje lentelėje ir pavyzdžiuose
The atominis tūris santykinė vertė, rodanti santykį tarp elemento molinės masės ir jos tankio. Taigi, šis tūris priklauso nuo elemento tankio, o tankis priklauso nuo fazės ir nuo to, kaip atomai yra išdėstyti šioje srityje..
Taigi Z elemento atominis tūris kitoje fazėje skiriasi nuo to, kuris yra kambario temperatūroje (skystis, kietas arba dujinis) arba kai jis yra tam tikrų junginių dalis. Taigi Z junginio atominis tūris junginyje ZA skiriasi nuo Z junginio ZB.

Kodėl? Norint tai suprasti, būtina palyginti atomus su, pavyzdžiui, rutuliukais. Marmuras, kaip ir aukščiausios kokybės mėlynos, labai gerai apibrėžė savo materialią sieną, kuri pastebima dėl jo ryškaus paviršiaus. Priešingai, atomų riba yra difuzinė, nors jie gali būti laikomi nuotoliniu būdu sferinėmis.
Taigi tai, kas lemia tašką, viršijančią atominę ribą, yra nulinė tikimybė surasti elektroną, ir šis taškas gali būti arčiau ar arčiau branduolio priklausomai nuo to, kiek kaimyninių atomų yra sąveikaujant atomui..
Indeksas
- 1 Atominis tūris ir spindulys
- 2 Papildoma formulė
- 3 Kaip periodinės lentelės atominis tūris skiriasi?
- 3.1 Pereinamųjų metalų atominiai tūriai
- 4 Pavyzdžiai
- 4.1 1 pavyzdys
- 4.2 2 pavyzdys
- 5 Nuorodos
Atominis tūris ir spindulys
Sąveikaujant dviem H atomams H molekule2, nustatomos jų branduolių pozicijos, taip pat atstumai tarp jų (tarpmiestiniai atstumai). Jei abu atomai yra sferiniai, spindulys yra atstumas tarp branduolio ir difuzinės ribos:
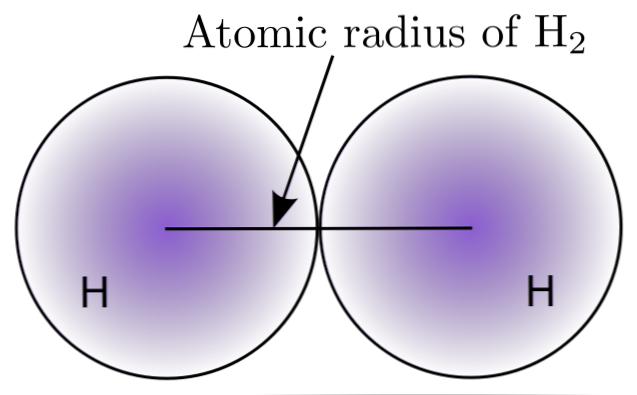
Viršutiniame paveiksle matyti, kaip elektrono radimo tikimybė mažėja, kai ji juda nuo branduolio. Skiriant tarpinį branduolį tarp dviejų, gaunamas atominis spindulys. Toliau, darant prielaidą, kad atomų sferinė geometrija, mes naudojame formulę, kad apskaičiuotume sferos tūrį:
V = (4/3) (Pi) r3
Šioje išraiškoje r yra H molekului nustatytas atominis spindulys2. Pagal šią netikslią metodą apskaičiuota V vertė gali keistis, jei, pavyzdžiui, buvo laikoma H2 skystoje arba metalinėje būsenoje. Tačiau šis metodas yra labai netikslus, nes atomų formos yra toli nuo idealios jų sąveikos srities..
Siekiant nustatyti kietųjų medžiagų atominius tūrius, atsižvelgiama į daugybę kintamųjų, susijusių su išdėstymu, ir jie gaunami rentgeno spindulių difrakcijos tyrimais..
Papildoma formulė
Molinė masė išreiškia medžiagos kiekį, turintį vieną molį cheminio elemento atomų.
Jo vienetai yra g / mol. Kita vertus, tankis yra tūris, užimantis vieną gramą elemento: g / ml. Kadangi atominio tūrio vienetai yra ml / mol, jūs turite žaisti su kintamaisiais, kad pasiektumėte norimus vienetus:
(g / mol) (ml / g) = ml / mol
Arba tas pats:
(Molinė masė) (1 / D) = V
(Molinė masė / D) = V
Taigi elemento vieno atomo molo tūris gali būti lengvai apskaičiuojamas; o su sferinio tūrio formule apskaičiuojamas atskiro atomo tūris. Norint pasiekti šią vertę iš pirmojo, reikia konversijos per Avogadro numerį (6.02 · 10).-23).
Kaip atomo tūris periodinėje lentelėje skiriasi?
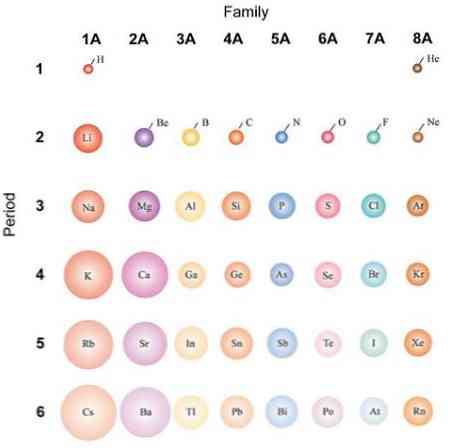
Jei atomai laikomi sferiniais, jų variacijos bus tokios pačios, kaip ir atomų spinduliuose. Viršutiniame vaizde, kuriame parodyti reprezentatyvūs elementai, iliustruojama, kad iš dešinės į kairę atomų nykštukė; vietoj to, iš viršaus į apačią, jie tampa vis didesni.
Taip yra todėl, kad tuo pačiu laikotarpiu branduolys įtraukia protonus, kai jis juda į dešinę. Šie protonai turi patrauklią jėgą išoriniams elektronams, kurie jaučia efektyvų branduolinį krūvį Zef, mažesnis nei faktinis branduolinis mokestis Z.
Vidinių sluoksnių elektronai atstumia išorinio sluoksnio elektronus, mažindami branduolio poveikį šiems; Tai žinoma kaip ekrano efektas. Tuo pačiu laikotarpiu ekrano efektas nesugeba neutralizuoti protonų skaičiaus didėjimo, todėl vidiniame sluoksnyje esantys elektronai neužkerta kelio atomų susitraukimui.
Tačiau nusileidžiant į grupę, įjungiami nauji energijos lygiai, leidžiantys elektronams orbituoti toliau nuo branduolio. Taip pat padidėja elektronų skaičius vidiniame sluoksnyje, kurio ekranavimo efektai pradeda mažėti, jei branduolys vėl prideda protonų.
Dėl šių priežasčių galima pastebėti, kad 1A grupė turi didžiausią atomų kiekį, skirtingai nuo mažų 8A grupės (arba 18) atomų, tauriųjų dujų..
Pereinamųjų metalų atominiai tūriai
Pereinamųjų metalų atomai įtraukia elektronus prie vidinių orbitų d. Šis ekrano efekto padidėjimas, o taip pat ir realus branduolinis mokestis Z, yra panaikinamas beveik vienodai, kad jų atomai išliktų panašūs dydžiai tuo pačiu laikotarpiu.
Kitaip tariant, per vieną laikotarpį pereinamieji metalai turi panašius atominius tūrius. Tačiau šie nedideli skirtumai yra labai svarbūs apibrėžiant metalinius kristalus (tarsi jie būtų metalo rutuliukai).
Pavyzdžiai
Yra dvi matematinės formulės elemento atominiam tūriui apskaičiuoti, kiekvienas iš jų turi atitinkamus pavyzdžius.
1 pavyzdys
Atsižvelgiant į vandenilio atominį spindulį -37 pm (1 pikometras = 10)-12m) - ir cezio -265 pm - apskaičiuoja jo atominius tūrius.
Naudodami sferinio tūrio formulę, mes turime:
VH= (4/3) (3.14) (37 val.)3= 212,07 pm3
VCs= (4/3) (3.14) (265 val.)3= 77912297,67 pm3
Tačiau šie tūriai, išreikšti pirometrais, yra pernelyg dideli, todėl jie transformuojami į angstremų vienetus, juos padauginus iš konversijos koeficiento (1 / 100pm).3:
(212.07 val3) (1 / 100pm)3= 2,1207 × 10-4 Å3
(77912297,67 val3) (1 / 100pm)3= 77,912 Å3
Taigi, mažo H atomo ir didžiojo C atomo atotrūkio dydžių skirtumai išlieka skaičiai akivaizdūs. Reikia nepamiršti, kad šie skaičiavimai yra tik apytiksliai pagal teiginį, kad atomas yra visiškai sferinis, kuris klajoja tikrovės akivaizdoje.
2 pavyzdys

Gryno aukso tankis yra 19,32 g / ml, o jo molinė masė yra 196,97 g / mol. Taikant formulę M / D vieno molio aukso atomų skaičiui apskaičiuoti yra:
VAu= (196,97 g / mol) / (19,32 g / ml) = 10,19 ml / mol
Tai reiškia, kad 1 molis aukso atomų užima 10,19 ml, bet kokio kiekio aukso atomas užima konkrečiai? Ir kaip ją išreikšti pm vienetais3? Todėl tiesiog naudokite šiuos konversijos koeficientus:
(10,19 ml / mol) · (mol / 6.02 · 10)-23 atomai) · (1 m / 100 cm)3· (13 val-12m)3= 16,92 · 106 pm3
Kita vertus, aukso atominis spindulys yra 166 pm. Jei lyginate abu tomus - tą, kuris buvo gautas pagal ankstesnį metodą, ir tą, kuris apskaičiuojamas pagal sferinio tūrio formulę, pamatysite, kad jie neturi tos pačios vertės:
VAu= (4/3) (3.14) (166 val.)3= 19,15 · 106 pm3
Kuris iš šių dviejų yra arčiausiai priimtinos vertės? Tai, kas yra arčiausiai eksperimentinių rezultatų, gautų kristalinės aukso struktūros rentgeno difrakcijos būdu.
Nuorodos
- Helmenstine, Anne Marie, Ph.D. (2017 m. Gruodžio 09 d.). Atominės apimties apibrėžimas. Gauta 2018 m. Birželio 6 d., Nuo: thinkco.com
- Mayfair, Andrew. (2018 m. Kovo 13 d.). Kaip apskaičiuoti Atomo tūrį. Moksliniai tyrimai. Gauta 2018 m. Birželio 6 d., Iš: sciencing.com
- „Wiki Kids Ltd.“ (2018 m.). Lothar Meyer atominės tūrio kreivės. Gauta 2018 m. Birželio 6 d. Iš: wonderwhizkids.com
- Lumen Periodinės tendencijos: atominis spindulys. Gauta 2018 m. Birželio 6 d. Iš: courses.lumenlearning.com
- Camilo J. Derpich. Tūris ir atominis tankis. Gauta 2018 m. Birželio 6 d., Nuo: es-puraquimica.weebly.com
- Whitten, Davis, Peck & Stanley. Chemija (8-asis red.). CENGAGE mokymasis, p. 222-224.
- CK-12 fondas. (2010 m. Vasario 22 d.). Lyginamieji atominiai dydžiai. [Pav.] Gauta 2018 m. Birželio 6 d., Iš: commons.wikimedia.org
- CK-12 fondas. (2010 m. Vasario 22 d.). H atomo spindulys2. [Pav.] Gauta 2018 m. Birželio 6 d., Iš: commons.wikimedia.org


