Atominis spindulys, kaip jis matuojamas, kaip jis keičiasi periodinėje lentelėje, pavyzdžiai
The atominis spindulys tai yra svarbus periodinių lentelės elementų periodinių savybių parametras. Jis yra tiesiogiai susijęs su atomų dydžiu, nes didesniu spinduliu yra didesnis arba stambesnis. Be to, jis yra susijęs su tos pačios elektroninės charakteristikos.
Kol atomas turi daugiau elektronų, tuo didesnis jo dydis ir atominis spindulys. Abu yra apibrėžti valentinio korpuso elektronai, nes atstumu, viršijančiu jų orbitą, tikimybė rasti elektroną artėja prie nulio. Priešinga vieta yra šalia branduolio: tikimybė surasti elektroną padidėja.

Viršutinis vaizdas reiškia medvilnės kamuoliukų pakuotę. Atkreipkite dėmesį, kad kiekvienas iš jų yra apsuptas šešių kaimynų, neskaitant kitos galimos viršutinės ar apatinės eilutės. Kaip suspausti medvilnės rutuliukai nustatys jų dydžius ir todėl jų spindulius; kaip ir atsitiktinai su atomais.
Elementai pagal jų cheminę prigimtį vienaip ar kitaip sąveikauja su savo atomais. Todėl atomo spindulio dydis kinta priklausomai nuo esamos jungties tipo ir jo atomų kieto pakavimo.
Indeksas
- 1 Kaip matuojamas atominis spindulys?
- 1.1 Branduolinio atstumo nustatymas
- 1,2 vienetai
- 2 Kaip jis keičia periodinę lentelę?
- 2.1 Per laikotarpį
- 2.2 Mažėjantis pagal grupę
- 2.3 Lantanido susitraukimas
- 3 Pavyzdžiai
- 4 Nuorodos
Kaip matuojamas atominis spindulys?
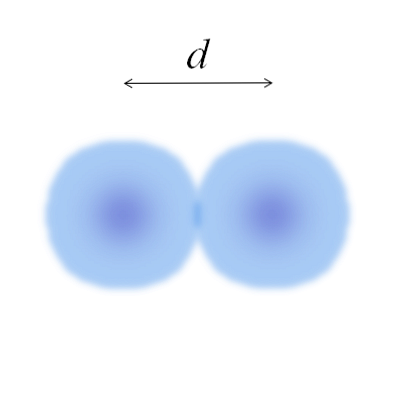
Pagrindiniame vaizde gali būti lengva matuoti medvilnės kamuoliukų skersmenį ir tada padalinti jį dviem. Tačiau atomo rutulys nėra visiškai apibrėžtas. Kodėl? Kadangi elektronai cirkuliuoja ir išsklaido tam tikrose erdvės vietose: orbitose.
Todėl atomas gali būti laikomas sfera, turinčia nepriekaištingus kraštus, kurių neįmanoma pasakyti už tai, kiek jie baigiasi. Pavyzdžiui, viršutiniame vaizde centrinis regionas, šalia branduolio, atrodo intensyviau, o jo kraštai yra neryškūs.
Vaizdas reiškia diatominę molekulę E2 (kaip Cl2, H2, O2, ir tt). Darant prielaidą, kad atomai yra sferiniai kūnai, jei atstumas buvo nustatytas d kuris atskiria abu branduolius kovalentinėje jungtyje, tuomet pakaks jį padalyti į dvi dalis (d/ 2) gauti atominį spindulį; tiksliau, E kovalentinis spindulys E2.
Ir jei E nesudaro kovalentinių ryšių su savimi, bet tai yra metalo elementas? Tada d tai būtų nurodoma kaimynų, kurie supa E metalinę konstrukciją, skaičiumi; tai yra atomo koordinavimo numeris (N.C) pakuotėje (prisiminkite pagrindinio vaizdo medvilnės kamuoliukus).
Tarptautinio atstumo nustatymas
Nustatyti d, Tai yra dviejų branduolių, esančių molekulėje arba pakuotėje, tarpinis branduolinis atstumas, jam reikia fizinės analizės metodų.
Vienas iš dažniausiai naudojamų yra rentgeno spindulių difrakcija, kurioje spinduliuojama šviesos spinduliuotė per kristalą, ir tiriamas difrakcijos modelis, atsirandantis dėl elektronų ir elektromagnetinės spinduliuotės sąveikos. Priklausomai nuo pakuotės, galima gauti skirtingus difrakcijos modelius, taigi ir kitas vertes d.
Jei atomai yra „įtempti“ kristalų grotelėse, jie parodys skirtingas vertes d palyginti su tuo, ką jie turėtų, jei jie būtų „patogūs“. Be to, šie tarpmiestiniai atstumai gali svyruoti vertėse, todėl atominis spindulys iš tikrųjų susideda iš vidutinės tokių matavimų vertės..
Kaip yra susijęs atominis spindulys ir koordinavimo numeris? V. Goldschmidt užmezgė ryšį tarp šių dviejų, kurių santykinė vertė N.C yra 12; nuo 0,97 pakuotei, kur atomas turi N.C lygus 8; 0,96, N.C lygus 6; ir 0,88 N.C iš 4.
Vienetai
Iš N.C reikšmių, lygių 12, buvo sudaryta daug lentelių, lyginant visų periodinės lentelės elementų atominius spindulius.
Kadangi ne visi elementai sudaro tokias kompaktiškas struktūras (N.C mažiau nei 12), V. Goldschmidt santykis naudojamas jų atominiams spinduliams apskaičiuoti ir išreikšti tą pačią pakuotę. Tokiu būdu atominių spindulių matavimai yra standartizuoti.
Bet kokiais vienetais jie išreiškia save? Nuo d yra labai mažas, turėtų būti naudojamas angstrom vienetams Å (10 ∙ 10-10m) arba plačiai naudojamas, pikometras (10 ∙ 10-12m).
Kaip jis keičia periodinę lentelę?
Per visą laikotarpį
Metaliniams elementams nustatyti atominiai spinduliai nurodomi kaip metaliniai spinduliai, o tų nemetalinių elementų - kovalentinių spindulių (pvz., Fosforo, P4, arba siera, S8). Tačiau tarp abiejų radijo tipų yra ryškesnis skirtumas nei pavadinimas.
Tuo pačiu laikotarpiu iš kairės į dešinę branduolys prideda protonų ir elektronų, tačiau pastarieji yra tik tokie patys energijos lygiai (pagrindinis kvantinis skaičius). Dėl to branduolys patiria didėjantį efektyvų branduolinį krūvį valentinių elektronų, kurie sudaro atominį spindulį, atžvilgiu.
Tokiu būdu tuo pačiu laikotarpiu nemetaliniai elementai turi mažesnius atominius (kovalentinius) spindulius nei metalai (metaliniai spinduliai)..
Mažėjantis pagal grupę
Mažėjant grupei, įjungiami nauji energijos lygiai, leidžiantys elektronams turėti daugiau vietos. Taigi, elektroninis debesis apima didesnius atstumus, jo neryškus periferija nustoja daugiau nukrypti nuo branduolio, todėl atominis spindulys plečiasi.
Lantanido susitraukimas
Vidinio sluoksnio elektronai padeda apsaugoti valentinių elektronų efektyvų branduolinį krūvį. Kai orbitos, sudarančios vidinius sluoksnius, turi daug „skylių“ (mazgų), kaip ir f orbitaliuose, branduolys stipriai sutaria atominį spindulį dėl prastos orbitalių ekranavimo..
Šį faktą patvirtina periodinio stalo 6-ojo laikotarpio lantanido susitraukimas. Nuo La iki Hf yra reikšmingas atomų spindulio, kurį sukelia orbitos f, kurios „užpildo“, kaip vienas eina per bloką f: lantanoidų ir aktinoidų, susitraukimas.
Panašus efektas taip pat gali būti pastebėtas ir nuo 4-ojo bloko bloko elementų. Šį kartą orbitų d silpno ekranavimo efektas, užpildantis pereinamųjų metalų laikotarpius..
Pavyzdžiai
Periodinės lentelės 2 laikotarpiui jos elementų atominiai spinduliai yra:
-Li: 257 val
-Būkite: 112 val
-B: 88 val
-C: 77 val
-N: 74 val
-O: 66 val
-F: 64 val.
Atkreipkite dėmesį, kad ličio metalas turi didžiausią atominį spindulį (257 m.), O fluoras, esantis tolimiausio laikotarpio dešinėje, yra mažiausias iš jų (64 val.). Tuo pačiu laikotarpiu atomo spindulys nusileidžia iš kairės į dešinę, o išvardytos vertės rodo.
Ličio, formuojant metalines jungtis, jo spindulys yra metalinis; ir fluoras, nes jis sudaro kovalentinius ryšius (F-F), jo spindulys yra kovalentinis.
Ir jei norite išreikšti atomines radijas angstromų vienetais? Tiesiog padalinkite juos 100: (257/100) = 2,57Å. Ir taip toliau su kitomis vertėmis.
Nuorodos
- Chemija 301. Atominės spindulys. Gauta iš: ch301.cm.utexas.edu
- CK-12 fondas. (2016 m. Birželio 28 d.). Atominis spindulys. Gauta iš: chem.libretexts.org
- Atominių spindulių tendencijos. Paimta iš: intro.chem.okstate.edu
- „Clackamas Community College“. (2002). Atominis dydis. Gauta iš: dl.clackamas.edu
- Clark J. (2012 m. Rugpjūčio mėn.). Atominis ir joninis spindulys. Gauta iš: chemguide.co.uk
- Shiver & Atkins. (2008). Neorganinė chemija (Ketvirtas leidimas., P. 23, 24, 80, 169). Mc Graw kalnas.


