Būdingos apolinės molekulės, kaip jas identifikuoti ir pavyzdžiai
The apolinės molekulės jie yra tie, kurie savo struktūroje pateikia simetrišką jų elektronų pasiskirstymą. Tai įmanoma, jei jo atomų elektronegatyvumo skirtumas yra mažas, arba jei elektronegatyvūs atomai ar grupės atima jų poveikį molekulėje.
Ne visada „absoliutus“ yra absoliutus. Dėl šios priežasties polinės poliškumo molekulės kartais laikomos apolinėmis; tai yra, dipolinis momentas μ arti 0. Čia įeina į santykinio reljefo reljefą: kiek maža turi būti μ, kad molekulė ar junginys būtų laikomas apoliniu?
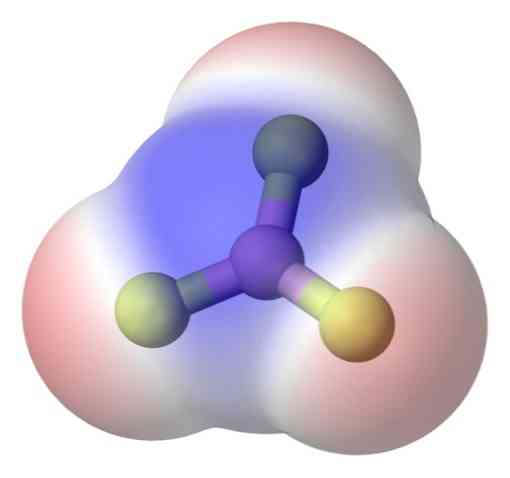
Kad geriau išspręstumėte šią problemą, turite boro trifluorido molekulę, BF3 (viršutinis vaizdas).
Fluoro atomas yra daug labiau elektroninis nei boro atomas, todėl B-F ryšys yra polinis. Tačiau BF molekulė3 yra simetriška (trigoninė plokštuma) ir apima trijų momentų B-F vektoriaus atšaukimą.
Taigi, taip pat susidaro apolinės molekulės, net ir esant poliarinėms jungtims. Sukurtą poliškumą gali subalansuoti kitas poliarinis ryšys, tokio pat dydžio kaip ir ankstesnis, bet orientuotas priešinga kryptimi; kaip tai atsitinka BF3.
Indeksas
- 1 Apolinės molekulės savybės
- 1.1. Simetrija
- 1.2. Elektronizavimas
- 1.3 Tarpmolekulinės jėgos
- 2 Kaip juos identifikuoti?
- 3 Pavyzdžiai
- 3.1. Grynosios dujos
- 3.2 Diatominės molekulės
- 3.3 Angliavandeniliai
- 3.4 Kita
- 4 Nuorodos
Apolinės molekulės savybės
Simetrija
Kad poliarinių ryšių poveikis vienas kitam būtų nutrauktas, molekulė turi turėti tam tikrą geometrinę struktūrą; pavyzdžiui, linijinė, lengviausia suprasti iš pirmo žvilgsnio.
Tai yra anglies dioksido (CO2), kuris turi dvi polines jungtis (O = C = O). Taip yra dėl to, kad du dipoliniai C = O nuorodų momentai vienas kitam atšaukia vienas kitą, o antrasis - į kitą, 180 ° kampu..
Todėl viena iš pirmųjų savybių, į kurias reikia atsižvelgti vertinant molekulės „apoliškumą“ kaip paukščio akį, yra stebėti, kaip ji yra simetriška..
Tarkime, kad vietoj CO2 turite COS molekulę (O = C = S), vadinamą karbonilo sulfidu.
Dabar ji nebėra apolinė molekulė, nes sieros elektronegatyvumas yra mažesnis nei deguonies; ir todėl dipolio momentas C = S skiriasi nuo C = O. Kaip rezultatas, COS yra polinė molekulė (kaip poliarai yra iš kitų maišų).
Apatinis vaizdas grafiškai apibendrinamas viskas, ką ką tik aprašyta:
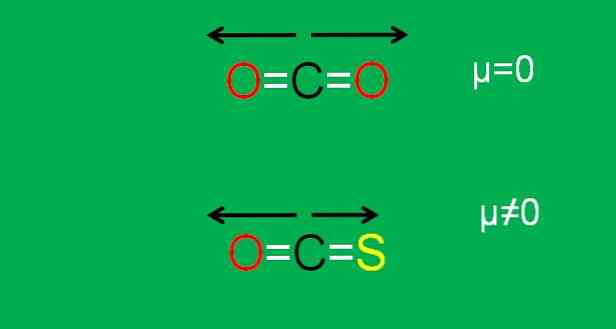
Atkreipkite dėmesį, kad C = S jungties dipolio momentas yra mažesnis nei C = O ryšys COS molekulėje.
Elektronegatyvumas
Elektroninis priskyrimas Paulingo skalėje turi reikšmes tarp 0,65 (franko) ir 4,0 (fluorui). Apskritai, halogenai turi didelį elektronegatyvumą.
Kai kovalentinį ryšį sudarančių elementų elektronegatyvumo skirtumas yra mažesnis arba lygus 0,4, sakoma, kad jis yra apolinis arba ne polinis. Tačiau vienintelės iš tiesų apolinės molekulės yra tos, kurios susidaro tarp identiškų atomų (pvz., Vandenilis, H-H)..
Tarpmolekulinės jėgos
Kad medžiaga ištirptų vandenyje, ji turi sąveikauti su elektrostatinėmis molekulėmis; sąveikos, kurios negali padaryti apolinių molekulių.
Apolinėse molekulėse jų elektros įkrovos nėra viename molekulės gale, bet paskirstytos simetriškai (arba vienodai). Todėl ji negali sąveikauti per dipolio-dipolio jėgas.
Priešingai, apolinės molekulės tarpusavyje sąveikauja per Londono dispersijos jėgas; tai yra momentiniai dipoliai, kurie poliarizuoja gretimų molekulių atomų elektroninį debesį. Čia molekulinė masė yra pagrindinis šių molekulių fizikinių savybių faktorius.
Kaip juos identifikuoti?
-Galbūt vienas iš geriausių metodų apolinės molekulės atpažinimui yra jo tirpumas skirtinguose poliariniuose tirpikliuose, paprastai juose blogai tirpstantis..
-Apoliarinės molekulės paprastai yra dujinės. Jie taip pat gali sudaryti su vandeniu nesimaišančius skysčius.
-Apolinių kietųjų dalelių savybė yra minkšta.
-Dispersijos jėgos, laikančios jas kartu, paprastai yra silpnos. Dėl to jų lydymosi arba virimo taškai yra mažesni nei poliarinio junginio.
-Apolinės molekulės, ypač skystos formos, yra prastos elektros laidininkės, nes joms trūksta elektros energijos.
Pavyzdžiai
Noble dujos
Nors jie nėra molekulės, tauriosios dujos laikomos apolinėmis. Darant prielaidą, kad du trumpus laikotarpius du jo atomai sąveikauja, He-He, ši sąveika gali būti laikoma (pusė) kaip molekulė; molekulė, kuri būtų apolinė.
Diatominės molekulės
Diatominės molekulės, tokios kaip H2, Br2, I2, Cl2, O2, ir F2, jie yra apoliniai. Jie turi bendrą formulę A2, A-A.
Angliavandeniliai
Ką daryti, jei A būtų atomų grupė? Tai būtų prieš kitus apolinius junginius; pavyzdžiui, etanas, CH3-CH3, kurio anglies skeletas yra tiesinis, C-C.
Metanas, CH4, ir etanas, C2H6, jos yra apolinės molekulės. Anglies elektregatyvumas yra 2,55; o vandenilio elektronegatyvumas yra 2.2. Todėl yra mažo intensyvumo dipolio vektorius, orientuotas nuo vandenilio iki anglies.
Tačiau, atsižvelgiant į metano ir etano molekulių geometrinę simetriją, jų molekulių dipolių vektorių arba dipolių momentų suma yra lygi nuliui, todėl molekulėse nėra neto mokesčio..
Apskritai tas pats pasakytina ir apie visus angliavandenilius, ir net jei jame yra nesočiųjų (dvigubos ir trigubos jungtys), jie laikomi apoliniais arba žemo poliškumo junginiais. Taip pat cikliniai angliavandeniliai yra apolinės molekulės, tokios kaip cikloheksanas arba ciklobutanas..
Kiti
Anglies dioksido molekulės (CO2) ir anglies disulfidas (CS)2) yra apolinės molekulės, kurios abi turi linijinę geometriją.
Anglies disulfido atveju anglies elektronegatyvumas yra 2,55, o sieros elektronegatyvumas yra 2,58; taip, kad abu elementai praktiškai turi tą patį elektronegatyvumą. Dipolio vektoriaus kartos nėra, todėl grynasis įkrovimas yra nulis.
Taip pat turime šias CCl molekules4 ir AlBr3, abu apoliniai:
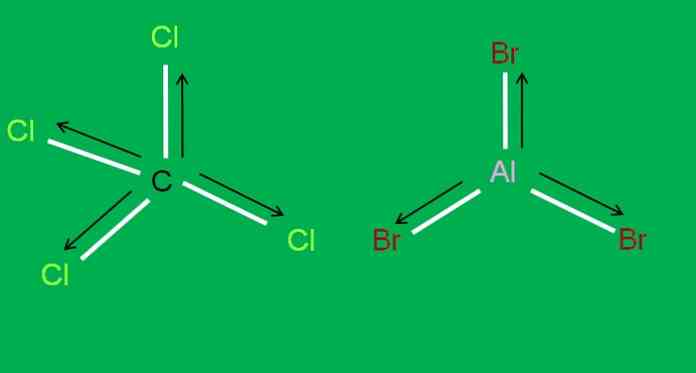
Aliuminio tribromide, AlBr3 tai atsitinka taip pat, kaip ir BF3, straipsnio pradžioje. Tuo tarpu anglies tetrachlorido, CCl4, geometrija yra tetraedrinė ir simetriška, nes visos C-Cl nuorodos yra lygios.
Panašiai ir molekulės, turinčios bendrąją formulę CX4 (CF4, CI4 ir CBr4), jie taip pat yra apoliniai.
Galiausiai, apolinė molekulė gali turėti net oktaedrinę geometriją, kaip ir sieros heksafluorido, SF.6. Tiesą sakant, ji gali turėti bet kokią geometriją ar struktūrą, jei ji yra simetriška ir jos elektroninis platinimas yra vienodas.
Nuorodos
- Carey F. A. (2008). Organinė chemija Karboksirūgštys. (Šeštasis leidimas). Mc Graw kalnas.
- Cedrón J., Landa V., Robles J. (2011). Molekulių poliškumas. Gauta iš: corinto.pucp.edu.pe
- Tutor Vista. (2018). Nepolinė molekulė. Gauta iš: chemistry.tutorvista.com
- Helmenstine, Anne Marie, Ph.D. (2019 m. Sausio 28 d.). Poliarinių ir ne poliarinių molekulių pavyzdžiai. Gauta iš: thinkco.com
- Kurtus R. (2016 m. Rugsėjo 19 d.). Poliarinės ir ne polinės molekulės. Čempionų mokykla. Gauta iš: school-for-champions.com
- Ganong W. (2004). Medicinos fiziologija 19 leidimasª. Šiuolaikinio vadovo redakcija.


