Kalorimetrų istorija, dalys, tipai ir jų charakteristikos
The kalorimetras yra įtaisas, naudojamas matuoti specifinės šilumos medžiagos (paprastai vandens) kiekio temperatūros pokyčius. Šį temperatūros pokytį lemia tiriamame procese absorbuojama arba išsiskirianti šiluma; cheminė medžiaga, jei tai yra reakcija, arba fizinis, jei jis susideda iš fazės ar būsenos pasikeitimo.
Laboratorijoje paprasčiausias randamas kalorimetras yra kavos puodelis. Jis naudojamas matuoti šilumą, sugeriamą arba išleistą į reakciją esant pastoviam slėgiui vandeniniame tirpale. Reakcijos pasirenkamos siekiant išvengti reagentų ar dujinių produktų įsikišimo.
 Eksoterminėje reakcijoje išsiskyręs šilumos kiekis gali būti apskaičiuojamas pagal kalorimetro ir vandeninio tirpalo temperatūros padidėjimą:
Eksoterminėje reakcijoje išsiskyręs šilumos kiekis gali būti apskaičiuojamas pagal kalorimetro ir vandeninio tirpalo temperatūros padidėjimą:
Reakcijos metu išsiskiriančios šilumos kiekis = kalorimetro sugeriamos šilumos kiekis ir tirpalo sugeriamos šilumos kiekis
Kalorimetro sugeriamos šilumos kiekis vadinamas kalorimetro kaloringumu. Tai nustatoma tiekiant tam tikrą vandens kiekį kalorimetrui žinomą šilumos kiekį. Tada matuojamas kalorimetro temperatūros padidėjimas ir jame esantis tirpalas.
Remiantis šiais duomenimis ir naudojant specifinę vandens šilumą (4.18 J / g.ºC), galima apskaičiuoti kalorimetro kaloringumą. Šis pajėgumas taip pat vadinamas pastoviu kalorimetru.
Kita vertus, vandeninio tirpalo gaunama šiluma yra lygi m · ce · Δt. Formuluotėje m = vandens masė, ce = specifinė vandens šiluma ir Δt = temperatūros kitimas. Visa tai žinant, galima apskaičiuoti eksoterminės reakcijos išskiriamą šilumą.
Indeksas
- 1 Kalorimetro istorija
- 2 dalys
- 3 Tipai ir jų charakteristikos
- 3.1 Kavos puodelis
- 3.2 Kalorimetrinis siurblys
- 3.3 Adiabatinis kalorimetras
- 3.4 Izoperibolinis kalorimetras
- 3.5 Srauto kalorimetras
- 3.6 Diferencinio skenavimo kalorimetrijos kalorimetras
- 4 Programos
- 4.1 Fizikochemijoje
- 4.2 Biologinėse sistemose
- 4.3 Deguonies siurblio kalorimetras ir kalorijų galia
- 5 Nuorodos
Kalorimetro istorija
1780 m. Prancūzų chemikas A. L. Lavoisieris, laikomas vienu iš chemijos tėvų, naudojo jūrų kiaulytę, kad matuotų šilumos gamybą savo kvėpavimu.
Kaip? Naudojant prietaisą, panašų į kalorimetrą. Jūrų kiaulytės šilumą patvirtino aparato apliejusio sniego lydymas.
Mokslininkai A.L Lavoisier (1743-1794) ir P. S. Laplaslas (1749-1827) suprojektavo kalorimetrą, kuris buvo naudojamas tam, kad būtų matuojama konkreti kūno šiluma ledo lydymo metodu..
Kalorimetras sudarytas iš alavo padengtos cilindrinės stiklinės, lakuotos, laikomos trikojiu ir vidiniu būdu nutrauktas piltuvu. Viduje, kitas stiklas buvo patalpintas, panašus į ankstesnį, su vamzdeliu, kuris buvo per išorinę kamerą ir kuris buvo su raktu. Antrojo stiklo viduje buvo tinklelis.
Šiame tinkle buvo patalpinta esmė arba objektas, kurio specifinė šiluma buvo norima nustatyti. Ledas buvo patalpintas koncentrinių laivų viduje, kaip ir krepšelyje.
Kūno šiluma buvo sugeriama ledo, todėl susidarė susiliejimas. Ir surenkamas ledo lydymo skystojo vandens produktas, atveriantis vidinio stiklo raktą.
Galiausiai, sveriant vandenį, buvo žinoma išlydyto ledo masė.
Dalys
Dažniausiai naudojamas kalorimetras chemijos mokymo laboratorijose yra vadinamasis kavos puodelio kalorimetras. Šį kalorimetrą sudaro stiklinė, arba anijoninės medžiagos talpykla, turinti tam tikras izoliacines savybes. Šioje talpykloje vandeninis tirpalas dedamas su kūnu, kuris gamins arba sugeria šilumą.
Viršutinėje pakuotės dalyje yra izoliacinės medžiagos dangtis su dviem skylėmis. Viename matuoklyje matuojamas termometras, kuris matuoja temperatūros pokyčius, o kitame - maišytuvas, pageidautina iš stiklo medžiagos, kuris atlieka vandeninio tirpalo turinio judėjimo funkciją..
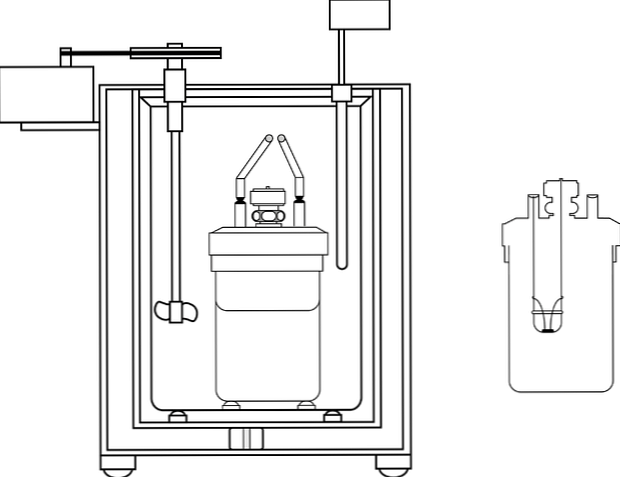
Vaizde matomos kalorimetrinio siurblio dalys; tačiau galima pastebėti, kad jis turi termometrą ir maišytuvą, bendrus elementus keliuose kalorimetruose.
Tipai ir jų ypatybės
Kavos puodelis
Tai yra tokia, kuri naudojama nustatant egzoterminės reakcijos išskiriamą šilumą, ir šiluma, absorbuojama endoterminėje reakcijoje..
Be to, jis gali būti naudojamas nustatant konkrečią kūno šilumą; tai yra šilumos kiekis, kurį turi sugerti gramas medžiagos, norint padidinti temperatūrą vienu Celsijaus laipsniu. .
Kalorimetrinis siurblys
Tai prietaisas, kuriame matuojamas šilumos kiekis, kuris išsiskiria arba sugeria į pastovaus tūrio reakciją.
Reakcija vyksta stipriame plieniniame inde (siurblyje), kuris yra panardintas į didelį vandens kiekį. Dėl to mažėja vandens temperatūros pokyčiai. Todėl daroma prielaida, kad su reakcija susiję pokyčiai matuojami esant pastoviai temperatūrai ir tūriui.
Pirmiau nurodyta, kad darbas atliekamas, kai reakcija vykdoma kalorimetriniame siurblyje.
Reakcija prasideda tiekiant elektros energiją per kabelius, prijungtus prie siurblio.
Adiabatinis kalorimetras
Jis pasižymi izoliacine konstrukcija, vadinama skydu. Skydas yra aplink kamerą, kurioje vyksta šilumos ir temperatūros pokyčiai. Jis taip pat yra prijungtas prie elektroninės sistemos, kuri išlaiko temperatūrą labai arti kameros temperatūros, kad būtų išvengta šilumos perdavimo.
Adiabatiniame kalorimetre minimalus temperatūros skirtumas tarp kalorimetro ir jo apylinkės; taip pat sumažinti šilumos perdavimo koeficientą ir šilumos mainų laiką.
Jos dalys susideda iš:
-Ląstelė (arba konteineris), integruota į izoliacijos sistemą, kuria siekiama išvengti šilumos nuostolių.
-Termometras matuoja temperatūros pokyčius.
-Šildytuvas, prijungtas prie valdomo elektros įtampos šaltinio.
-Ir skydas, jau paminėtas.
Šio tipo kalorimetruose galima nustatyti tokias savybes kaip entropija, Debye temperatūra ir elektroninis būsenos tankis.
Izoperibolinis kalorimetras
Tai įtaisas, kuriame reakcijos elementas ir siurblys yra panardinti į konstrukciją, vadinamą striukė. Tokiu atveju vadinamoji striukė susideda iš vandens, laikomos pastovioje temperatūroje.
Ląstelės ir siurblio temperatūra pakyla, kai degimo metu išsiskiria šiluma; tačiau vandens striukės temperatūra palaikoma fiksuotoje temperatūroje.
Mikroprocesorius kontroliuoja ląstelės ir striukės temperatūrą, atlikdamas būtinus nuotėkio šilumos koregavimus, atsirandančius dėl skirtumų tarp dviejų temperatūrų..
Šie koregavimai atliekami nepertraukiamai ir su galutine korekcija, remiantis matavimais prieš ir po bandymo.
Srauto kalorimetras
„Kalibro“ sukurtas įrenginys turi įrenginį, leidžiantį pastatyti dujas pastoviu greičiu. Pridedant šilumą, matuojamas skysčio temperatūros padidėjimas.
Srauto kalorimetras pasižymi:
- Tikslus pastovaus srauto matavimas.
- Tikslus šilumos kiekio matavimas į skystį per šildytuvą.
- Tikslus dujų suvartojimo temperatūros padidėjimo matavimas
- Konstrukcija, skirta matuoti slėgį turinčios dujos talpa.
Kalorimetras diferencinei skenavimo kalorimetrijai
Jis pasižymi dviem konteineriais: viename tiriamame mėginyje, o kitas laikomas tuščias arba naudojama etaloninė medžiaga..
Du laivai šildomi pastoviu energijos greičiu, naudojant du nepriklausomus šildytuvus. Kai prasideda abiejų konteinerių šildymas, kompiuteris suformuos šildytuvų šilumos srauto skirtumą nuo temperatūros, taip nustatydamas šilumos srautą..
Be to, galima nustatyti temperatūros svyravimus kaip laiko funkciją; ir galiausiai kalorijų pajėgumas.
Programos
Fizikochemijoje
-Pagrindiniai kalorimetrai, tipo kavos puodelis leidžia išmatuoti šilumos kiekį, kurį kūnas išskiria arba sugeria. Jie gali nustatyti, ar reakcija yra egzoterminė, ar endoterminė. Be to, galima nustatyti specifinę kūno šilumą.
-Su adiabatiniu kalorimetru buvo galima nustatyti cheminio proceso ir elektroninio valstybės tankio entropiją.
Biologinėse sistemose
-Mikrokalorimetrai naudojami tirti biologines sistemas, apimančias molekulių sąveiką, taip pat vykstančius molekulinius konformacinius pokyčius; pavyzdžiui, molekulės išsiskleidimo metu. Linija apima diferencinį nuskaitymą ir izoterminį titravimą.
-Mikrokalorimetras naudojamas mažų molekulių, bioterapinių preparatų ir vakcinų vaistų kūrimui.
Deguonies siurblio kalorimetras ir kalorijų galia
Daugelio medžiagų degimas vyksta deguonies siurblio kalorimetre, o jo kaloringumas gali būti nustatytas. Tarp medžiagų, tiriamų naudojant šį kalorimetrą, yra: anglis ir koksas; valgomieji aliejai, sunkūs ir lengvi; benzinas ir visi varikliai.
Kaip ir orlaivių reaktorių kuro rūšys; kuro atliekų ir atliekų šalinimas; Maisto produktai ir maisto papildai; pašariniai pašarai ir pašarai; statybinės medžiagos; raketų ir raketinio kuro.
Panašiai kalorijų galia buvo nustatyta deginamųjų medžiagų termodinaminiuose tyrimuose kalorimetrijoje; energijos balanso ekologijoje tyrime; sprogmenyse ir terminiuose milteliuose bei pagrindinių termodinaminių metodų mokyme.
Nuorodos
- Whitten, Davis, Peck & Stanley. Chemija (8-asis red.). Mokymosi mokymas.
- González J., Cortés L. & Sánchez A. (s.f.). Adiabatinė kalorimetrija ir jos taikymas. Susigrąžinta iš: cenam.mx
- Vikipedija. (2018). Kalorimetras. Gauta iš: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (2018 m. Birželio 22 d.). Kalorimetro apibrėžimas chemijoje. Gauta iš: thinkco.com
- Gillespie, Claire. (2018 m. Balandžio 11 d.). Kaip veikia kalorimetras? Moksliniai tyrimai. Gauta iš: sciencing.com


